pTH-RP (1-40) (human);AVSEHQLLHDKGKSIQDLRRRFFLHHLAIEIHTAEIRATS
pTH-RP (1-40) (human) 主要通过依赖PTH1R受体的信号通路发挥生理与病理作用,同时存在少量非受体依赖调控,具体机理分为三个层面:1. 受体结合与信号激活:该片段的N端1-34位氨基酸为PTH1R受体核心结合区域,可特异性结合细胞膜上的PTH1R受体,激活下游cAMP/PKA、IP3/Ca²⁺等信号通路,调控骨代谢相关基因的表达,进而促进破骨细胞活性、抑制成骨细胞凋亡,调节骨吸
一、基本性质
英文名称:pTH-RP (1-40) (human),Parathyroid Hormone-Related Protein (1-40) (human)
中文名称:人源甲状旁腺激素相关蛋白(1-40)
单字母多肽序列:AVSEHQLLHDKGKSIQDLRRRFFLHHLAIEIHTAEIRATS
三字母序列:Ala-Val-Ser-Glu-His-Gln-Leu-Leu-His-Asp-Lys-Gly-Lys-Ser-Ile-Gln-Asp-Leu-Arg-Arg-Arg-Phe-Phe-Leu-His-His-Leu-Ile-Ala-Glu-Ile-His-Thr-Ala-Glu-Ile-Arg-Ala-Thr-Ser
等电点(pI):理论值约9.42,属于强碱性多肽
分子式:C207H334N66O58
分子量:4675.35 Da
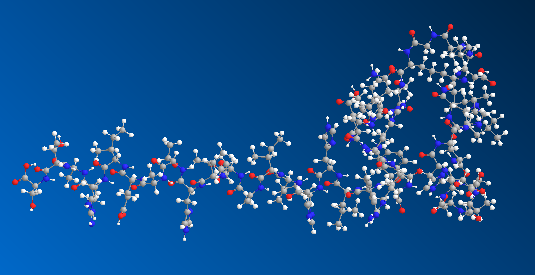
结构特征:含N端核心功能区域,富含碱性氨基酸(3个Lys、4个Arg、3个His),强碱性;含1个甲硫氨酸(Met),易被氧化;C端为游离丝氨酸(Ser),无酰胺化修饰;N端为丙氨酸(Ala),序列与人源PTHrP全长N端1-40片段完全一致,与PTH(甲状旁腺激素)N端序列高度同源,具备受体结合相关结构
CAS号:无明确单一CAS号(该片段为PTHrP全长的N端截短片段,主要作为科研用工具肽,无商业化通用CAS登记)
结构式:
二、应用领域与应用原理
应用领域主要聚焦于科研及药物研发辅助领域,核心包括三大方向:
1. 甲状旁腺激素相关蛋白(PTHrP)N端结构与功能研究,用于解析PTHrP N端(1-40)片段的受体结合能力及信号调控功能,明确其与PTH1R受体的相互作用机制
2. 骨代谢与钙磷稳态研究,用于骨质疏松、甲状旁腺功能异常、恶性肿瘤相关高钙血症的机制研究,探索该片段在骨吸收、骨形成调控中的作用;
3. 多肽药物研发辅助研究,作为工具肽用于PTH1R受体激动剂/拮抗剂筛选、相关特异性抗体研发、多肽药物构效关系分析,以及骨代谢相关药物的体外活性评价。
应用原理:pTH-RP (1-40) (human) 为PTHrP全长的N端截短片段,包含PTH1R受体的核心结合区域(1-34位氨基酸),可特异性结合PTH1R受体并激活经典信号通路,其功能发挥依赖自身结构特征——富含碱性氨基酸(Lys、Arg、His),可与PTH1R受体胞外结构域形成特异性相互作用,模拟内源性PTHrP的生理功能;该片段与人源体内内源性PTHrP N端序列完全一致,且与PTH N端序列高度同源,可作为工具肽模拟内源性PTHrP对骨代谢、钙磷稳态的调控作用,同时可用于区分PTH与PTHrP的受体结合差异,为相关机制研究及药物筛选提供可靠的实验材料。
三、作用机理
pTH-RP (1-40) (human) 主要通过依赖PTH1R受体的信号通路发挥生理与病理作用,同时存在少量非受体依赖调控,具体机理分为三个层面:1. 受体结合与信号激活:该片段的N端1-34位氨基酸为PTH1R受体核心结合区域,可特异性结合细胞膜上的PTH1R受体,激活下游cAMP/PKA、IP3/Ca²⁺等信号通路,调控骨代谢相关基因的表达,进而促进破骨细胞活性、抑制成骨细胞凋亡,调节骨吸收与骨形成的平衡;2. 骨代谢与钙磷稳态调控:激活PTH1R受体后,可促进肾脏对钙的重吸收、抑制磷的排泄,升高血钙水平,同时促进骨基质分解,释放钙磷,维持体内钙磷稳态,这一机制在恶性肿瘤相关高钙血症中尤为明显(肿瘤细胞分泌该片段,导致血钙异常升高);3. 辅助调控作用:该片段中的Met残基可参与细胞内氧化还原反应,间接影响细胞氧化应激水平,调控细胞增殖与分化;N端与中段的空间构象共同维持其与PTH1R受体的结合特异性,构象改变(如Met氧化、肽键水解)会显著降低其受体结合能力与信号激活效率;此外,该片段可通过调控破骨细胞与成骨细胞的活性平衡,参与骨质疏松、骨转移等疾病的病理过程。
四、药物研发相关
该多肽目前主要作为科研工具肽,同时为骨代谢相关多肽药物研发提供重要参考,核心研发价值体现在三个方面:1. 靶点验证:用于验证PTH1R受体及PTHrP N端片段是否可作为骨质疏松、恶性肿瘤相关高钙血症的潜在治疗靶点,通过调控该片段的表达或受体结合活性,观察骨代谢与钙磷稳态的变化,为新药研发提供靶点依据;2. 工具肽应用:作为标准对照肽,用于筛选针对PTH1R受体的高选择性激动剂/拮抗剂,评估候选药物的受体结合亲和力、信号激活效率,辅助优化药物结构(如延长半衰期、提高受体选择性);3. 药物设计参考:基于该片段的结构特征(PTH1R受体结合区域、Met氧化位点),为设计靶向PTH1R受体的长效、低副作用多肽药物提供参考,例如通过氨基酸定点突变替换易氧化的Met残基,提高药物稳定性,或修饰N端结构,增强受体结合特异性、延长体内半衰期;目前研发难点在于,该片段的受体选择性不足(与PTH共享PTH1R受体),高剂量易引发血钙升高、骨破坏等副作用,暂无相关候选药物进入临床试验阶段,研发重点集中在结构优化以提高受体选择性、降低副作用
五、研究进展
基础研究方面,目前已明确pTH-RP (1-40) 为PTHrP N端的核心功能片段,包含PTH1R受体结合区域,可有效激活PTH1R信号通路,调控骨代谢与钙磷稳态;研究证实,该片段在骨质疏松模型中可促进骨形成、改善骨密度,在恶性肿瘤(如乳腺癌、肺癌)中高表达,其表达水平与肿瘤相关高钙血症发生率呈正相关,沉默该片段的表达可显著降低血钙水平、减轻骨破坏;同时,研究发现该片段的Met残基氧化会显著降低其受体结合能力与信号激活效率,N端1-10位氨基酸为信号激活关键位点。临床前研究方面,已基于该片段开发出部分结构修饰类似物,通过氨基酸突变或化学修饰,提高其受体选择性与体内半衰期,在动物模型中展现出良好的骨代谢调控效果,可有效改善骨质疏松、降低肿瘤相关高钙血症的血钙水平,但尚未进入体内临床试验阶段。前沿研究方向主要包括:解析该片段与PTH1R受体的结合晶体结构,明确核心结合位点;探索该片段与其他骨代谢相关因子(如GLP-1、PYY)的交叉调控网络;优化该片段的结构,开发高选择性、长效的PTH1R受体激动剂/拮抗剂;研究该片段在不同疾病模型中的表达差异及功能异质性,为精准治疗提供新思路。目前整体研究仍处于基础与临床前阶段,尚未实现临床转化应用。
六、相关案例分析
案例1:pTH-RP (1-40) 对骨质疏松小鼠骨代谢的调控作用研究。研究背景:骨质疏松的核心病理特征为骨吸收大于骨形成,PTHrP可调控骨代谢,推测其N端片段(1-40)可改善骨质疏松。研究方法:构建去卵巢骨质疏松小鼠模型,分为pTH-RP (1-40) 给药组与对照组,持续给药4周后,检测小鼠骨密度、骨组织病理学变化,以及血清中骨代谢标志物(碱性磷酸酶、骨钙素)的水平。研究结果:给药组小鼠骨密度显著升高,骨组织破坏程度明显减轻,血清中碱性磷酸酶、骨钙素水平显著升高(提示骨形成增强)。研究结论:pTH-RP (1-40) 可通过激活PTH1R信号通路,促进骨形成、改善骨质疏松,为骨质疏松的治疗提供了新的思路与实验依据。
案例2:Met残基氧化对pTH-RP (1-40) 受体结合活性的影响研究。研究背景:该片段含1个Met残基,易被氧化,推测氧化会影响其受体结合能力与信号功能。研究方法:制备天然pTH-RP (1-40) 与Met氧化型片段,通过表面等离子体共振(SPR)实验检测两者与PTH1R受体的结合亲和力,通过细胞实验检测两者对下游cAMP信号通路的激活效率。研究结果:氧化型片段与PTH1R受体的结合亲和力较天然片段下降70%以上,对cAMP信号通路的激活效率显著降低,且氧化程度越高,活性越弱。研究结论:Met残基的氧化会显著降低pTH-RP (1-40) 的受体结合活性与信号激活能力,为该片段的储存、结构优化及药物设计提供了重要参考。
案例3:pTH-RP (1-40) 特异性拮抗剂对肿瘤相关高钙血症的抑制作用研究。研究背景:基于pTH-RP (1-40) 与PTH1R的结合机制,开发特异性拮抗剂,探索其对肿瘤相关高钙血症的治疗效果。研究方法:制备针对pTH-RP (1-40) 的多肽拮抗剂,建立肺癌相关高钙血症小鼠模型,分为拮抗剂治疗组与对照组,检测小鼠血钙水平、肿瘤生长情况及骨破坏程度。研究结果:拮抗剂治疗组小鼠的血钙水平显著降低,肿瘤生长受到一定抑制,骨破坏程度明显减轻,且无明显毒性反应。研究结论:pTH-RP (1-40) 特异性拮抗剂可通过阻断其与PTH1R受体的结合,抑制肿瘤相关高钙血症,为相关疾病的药物研发提供了实验基础。
更多推荐
 已为社区贡献6条内容
已为社区贡献6条内容







所有评论(0)