pTH-RP (1-34) (human) ;AVSEHQLLHDKGKSIQDLRRRFFLHHLAIEIHTA
基础研究方面,目前已明确pTH-RP (1-34) 是PTHrP介导生理功能的核心片段,包含PTH1R受体的完整结合与信号激活序列,可高效激活PTH1R信号通路,是调控骨代谢与钙磷稳态的关键分子;1. 受体结合与信号激活:该片段包含PTH1R受体的完整结合与信号激活序列,可特异性结合细胞膜上的PTH1R受体,高效激活下游cAMP/PKA、IP3/Ca²⁺等信号通路,调控骨代谢相关基因(如Runx2
一、基本性质
英文名称:pTH-RP (1-34) (human),Parathyroid Hormone-Related Protein (1-34) (human)
中文名称:人源甲状旁腺激素相关蛋白(1-34)
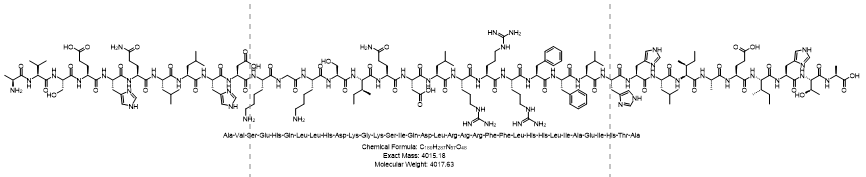
单字母多肽序列:AVSEHQLLHDKGKSIQDLRRRFFLHHLAIEIHTA
三字母序列:Ala-Val-Ser-Glu-His-Gln-Leu-Leu-His-Asp-Lys-Gly-Lys-Ser-Ile-Gln-Asp-Leu-Arg-Arg-Arg-Phe-Phe-Leu-His-His-Leu-Ile-Ala-Glu-Ile-His-Thr-Ala
等电点(pI):理论值约9.38,属于强碱性多肽
分子式:C180H287N57O48
分子量:4017.63 Da
CAS号:83445-62-1
溶解性相关基础特征:强碱性决定其易溶于极性溶剂(去离子水、酸性缓冲液),难溶于非极性溶剂,无Met残基故氧化稳定性较好,储存过程中主要需防范肽键水解。
结构式:
二、应用领域与应用原理
应用领域主要聚焦于科研、药物研发及骨代谢疾病研究,核心包括三大方向:
1. 甲状旁腺激素相关蛋白(PTHrP)核心功能区域研究,用于解析PTHrP 1-34片段与PTH1R受体的结合机制、信号激活规律,明确其在骨代谢调控中的核心作用
2. 骨代谢与钙磷稳态相关研究,用于骨质疏松、甲状旁腺功能亢进、恶性肿瘤相关高钙血症的机制研究,探索该片段在骨吸收、骨形成平衡调控中的具体作用
3. 多肽药物研发核心研究,作为工具肽与候选肽基础,用于PTH1R受体激动剂/拮抗剂筛选、多肽药物构效关系分析、骨代谢药物体外活性评价,以及相关特异性抗体研发。
应用原理:pTH-RP (1-34) (human) 为PTHrP全长的N端核心截短片段,是介导其生理功能的关键区域,包含PTH1R受体的完整结合与信号激活序列,可特异性结合PTH1R受体并高效激活经典信号通路;其功能发挥依赖自身强碱性结构特征——富含Lys、Arg、His等碱性氨基酸,可与PTH1R受体胞外结构域形成特异性静电相互作用与疏水相互作用,完美模拟内源性PTHrP的核心生理功能;该片段与人源体内内源性PTHrP N端1-34序列完全一致,且与PTH N端1-34序列高度同源,可作为工具肽用于区分PTH与PTHrP的受体结合差异,也可作为候选肽基础用于骨代谢药物研发,为相关机制研究及药物筛选提供可靠的实验材料。
三、作用机理
pTH-RP (1-34) (human) 主要通过依赖PTH1R受体的信号通路发挥核心生理与病理作用,是PTHrP介导骨代谢调控的关键片段,具体机理分为三个层面:
1. 受体结合与信号激活:该片段包含PTH1R受体的完整结合与信号激活序列,可特异性结合细胞膜上的PTH1R受体,高效激活下游cAMP/PKA、IP3/Ca²⁺等信号通路,调控骨代谢相关基因(如Runx2、OPG)的表达,进而促进破骨细胞分化与活性、抑制成骨细胞凋亡,精准调节骨吸收与骨形成的平衡
2. 骨代谢与钙磷稳态调控:激活PTH1R受体后,可促进肾脏近曲小管对钙的重吸收、抑制远曲小管对磷的排泄,升高血钙水平、降低血磷水平,同时促进骨基质分解,释放骨钙与骨磷,维持体内钙磷稳态,这一机制在恶性肿瘤相关高钙血症中尤为关键(肿瘤细胞过量分泌该片段,导致血钙异常升高
3. 结构与功能关联:该片段无甲硫氨酸(Met)残基,氧化稳定性显著优于含Met的PTHrP片段(如1-40片段),不易因氧化导致构象改变;N端1-10位氨基酸为信号激活关键位点,C端游离丙氨酸结构可维持其与PTH1R受体的结合特异性,肽键水解或末端结构修饰会显著降低其受体结合能力与信号激活效率;此外,该片段可通过调控破骨细胞与成骨细胞的活性平衡,参与骨质疏松、骨转移等疾病的病理过程。
四、药物研发相关
该多肽是PTHrP相关药物研发的核心工具肽与候选肽基础,核心研发价值体现在三个方面:
1. 靶点验证:用于验证PTH1R受体及PTHrP 1-34片段是否可作为骨质疏松、恶性肿瘤相关高钙血症、甲状旁腺功能亢进的潜在治疗靶点,通过调控该片段的表达或受体结合活性,观察骨代谢与钙磷稳态的变化,为新药研发提供明确靶点依据
2. 工具肽应用:作为标准对照肽,广泛用于筛选针对PTH1R受体的高选择性激动剂/拮抗剂,精准评估候选药物的受体结合亲和力、信号激活效率,辅助优化药物结构(如延长半衰期、提高受体选择性、降低脱靶效应)
3. 候选肽基础:该片段本身为PTHrP的核心功能区域,可通过化学修饰(如脂肪酸修饰、氨基酸定点突变)开发长效、高选择性的PTH1R受体激动剂,用于骨质疏松的治疗,相较于天然片段,修饰后可延长体内半衰期、降低给药频率;目前研发难点在于,该片段与PTH共享PTH1R受体,受体选择性不足,高剂量易引发血钙升高、骨过度吸收等副作用,部分修饰后的类似物已进入早期临床试验阶段,研发重点集中在结构优化以提高受体选择性、降低副作用、延长体内半衰期。
五、研究进展
基础研究方面,目前已明确pTH-RP (1-34) 是PTHrP介导生理功能的核心片段,包含PTH1R受体的完整结合与信号激活序列,可高效激活PTH1R信号通路,是调控骨代谢与钙磷稳态的关键分子;研究证实,该片段在骨质疏松模型中可显著促进骨形成、改善骨密度,在恶性肿瘤(如乳腺癌、肺癌、前列腺癌)中高表达,其表达水平与肿瘤相关高钙血症发生率呈正相关,沉默该片段的表达可显著降低血钙水平、减轻骨破坏;同时,研究发现该片段无Met残基,氧化稳定性较好,N端1-10位氨基酸为信号激活关键位点,C端结构修饰可显著影响其受体结合能力。临床前研究方面,已基于该片段开发出多种结构修饰类似物,通过脂肪酸酰化、氨基酸定点突变等方式,提高其体内半衰期与受体选择性,在动物模型中展现出良好的骨代谢调控效果,可有效改善骨质疏松、降低肿瘤相关高钙血症的血钙水平。临床研究方面,部分长效PTH1R受体激动剂(基于pTH-RP 1-34片段修饰)已进入Ⅰ、Ⅱ期临床试验,评估其在骨质疏松患者中的安全性、耐受性与疗效,初步结果显示可显著改善患者骨密度,且副作用可控;前沿研究方向主要包括:解析该片段与PTH1R受体的结合晶体结构,明确核心结合位点;探索该片段与其他骨代谢相关因子(如GLP-1、BMP-2)的交叉调控网络;优化该片段的结构,开发高选择性、长效、低副作用的PTH1R受体激动剂/拮抗剂;研究该片段在不同疾病模型中的表达差异及功能异质性,为精准治疗提供新思路。
六、相关案例分析
案例1:pTH-RP (1-34) 对骨质疏松小鼠骨代谢的调控作用研究。研究背景:骨质疏松的核心病理特征为骨吸收大于骨形成,pTH-RP 1-34作为PTHrP的核心功能片段,推测其可改善骨质疏松。研究方法:构建去卵巢骨质疏松小鼠模型,分为pTH-RP (1-34) 给药组与对照组,持续给药4周后,检测小鼠骨密度、骨组织病理学变化,以及血清中骨代谢标志物(碱性磷酸酶、骨钙素、抗酒石酸酸性磷酸酶)的水平。研究结果:给药组小鼠骨密度显著升高,骨组织破坏程度明显减轻,血清中碱性磷酸酶、骨钙素水平显著升高(提示骨形成增强),抗酒石酸酸性磷酸酶水平显著降低(提示骨吸收抑制)。研究结论:pTH-RP (1-34) 可通过激活PTH1R信号通路,平衡骨吸收与骨形成,有效改善骨质疏松,为骨质疏松的治疗提供了新的思路与实验依据。
案例2:pTH-RP (1-34) 结构修饰对其体内半衰期与活性的影响研究。研究背景:天然pTH-RP (1-34) 体内半衰期短(约30分钟),易被酶解,限制其临床应用,需通过结构修饰延长其半衰期。研究方法:对pTH-RP (1-34) 进行脂肪酸酰化修饰,制备长效类似物,对比天然片段与修饰后类似物在小鼠体内的半衰期、血药浓度变化,以及对骨密度的调控效果。研究结果:修饰后类似物体内半衰期延长至8小时以上,血药浓度维持稳定,对小鼠骨密度的提升效果显著优于天然片段,且无明显血钙异常升高副作用。研究结论:脂肪酸酰化修饰可有效延长pTH-RP (1-34) 的体内半衰期、增强其骨代谢调控活性,为其临床转化应用提供了重要参考。
案例3:pTH-RP (1-34) 特异性拮抗剂对肿瘤相关高钙血症的抑制作用研究。研究背景:肿瘤相关高钙血症的核心诱因是肿瘤细胞过量分泌PTHrP(主要为1-34片段),激活PTH1R受体导致血钙升高,开发该片段的特异性拮抗剂可用于疾病治疗。研究方法:制备针对pTH-RP (1-34) 的多肽拮抗剂,建立肺癌相关高钙血症小鼠模型,分为拮抗剂治疗组与对照组,检测小鼠血钙、血磷水平,肿瘤生长情况及骨破坏程度。研究结果:拮抗剂治疗组小鼠的血钙水平显著降低、血磷水平恢复正常,肿瘤生长受到一定抑制,骨破坏程度明显减轻,且无明显毒性反应。研究结论:pTH-RP (1-34) 特异性拮抗剂可通过阻断其与PTH1R受体的结合,有效抑制肿瘤相关高钙血症,为该疾病的药物研发提供了实验基础。
更多推荐
 已为社区贡献6条内容
已为社区贡献6条内容








所有评论(0)