紫杉醇的合成生物学技术路线综述--文献精读195
A synthetic biology roadmap for sustainable production of the plant-originated anti-cancer drug paclitaxel用于植物源抗癌药物紫杉醇可持续生产的合成生物学技术路线图紫杉醇生物合成机制研究进展-文献精读35_thmgr-CSDN博客近十年天然产物药物的生物合成研究进展-文献精读33_雌四醇合成工艺
A synthetic biology roadmap for sustainable production of the plant-originated anti-cancer drug paclitaxel
用于植物源抗癌药物紫杉醇可持续生产的合成生物学技术路线图
紫杉醇生物合成机制研究进展-文献精读35_thmgr-CSDN博客
近十年天然产物药物的生物合成研究进展-文献精读33_雌四醇合成工艺-CSDN博客
基因组挖掘指导天然药物分子的发现-文献精读34_plantismash-CSDN博客
紫杉醇的药物代谢-文献精读73_紫杉醇球棍模型-CSDN博客
药用植物的空间多组学:从生物合成途径到工业应用-文献精读51_药用植物多组学-CSDN博客

研究亮点
合成生物学工具(mpXsn、CRISPR 基因编辑技术、计算机模拟技术)推动紫杉醇中间体可持续生产的代谢途径解析与组装进程。非常规底盘生物(蓝细菌、枯草芽孢杆菌、丝状真菌)突破大肠杆菌、酵母及烟草的局限,为紫杉醇中间体的异源合成拓展了新选择。人工智能驱动的细胞色素 P450 单加氧酶 / 紫杉烯合成酶(P450/TXS)定向改造与合成模块构建,结合代谢工程技术,实现底盘生物中紫杉醇合成途径的优化。无细胞 - 化学酶法杂合合成技术可规避细胞色素 P450 的底物宽泛性与细胞毒性问题,高效合成紫杉醇中间体。人工合成微生物菌群(跨物种分工协作)显著提升紫杉醇中间体产量,突破单一菌株发酵的性能瓶颈。
摘要
紫杉醇是一种从红豆杉属植物中提取的临床高效抗癌药物,其可持续供应长期面临挑战。合成生物学为紫杉醇的从头合成提供了重要契机,尤其是近年来在解析其复杂生物合成途径方面取得的突破性进展,更是进一步拓宽了该技术的应用前景。然而,紫杉醇的异源生物合成仍受多重关键瓶颈制约,包括合成途径复杂、细胞色素 P450 表达效率低下、代谢流分配不合理等。本研究系统探讨了合成生物学技术在紫杉醇代谢途径解析与重构中的应用机制,并提出利用植物伴生蓝细菌、丝状真菌等非传统底盘生物提升细胞色素 P450 适配性的策略。同时,本研究构建了一套实用技术框架,整合无细胞合成系统、人工合成微生物菌群、化学酶法杂合合成及机器学习等前沿技术,为紫杉醇及其他天然产物的可持续生产提供解决方案。
紫杉醇可持续生产的技术与瓶颈
紫杉醇(商品名:泰素 ®)是一种提取自红豆杉属(紫杉)植物树皮的天然二萜类药物,其分子结构具有独特的 6/8/6 元碳环骨架,并带有丰富的含氧官能团与复杂的化学结构 [1]。作为一种临床应用广泛的广谱抗癌药物,紫杉醇被大量用于乳腺癌、卵巢癌及黑色素瘤的治疗 [2]。截至 2000 年,紫杉醇已成为全球销量最高的抗癌治疗药物,市场规模达到约 16 亿美元 [3]。然而,该药物在天然红豆杉树皮中的含量极低,仅占干重的 0.001%–0.050%,这导致天然红豆杉资源遭到严重破坏 [4]。这种资源稀缺性促使科研人员致力于开发紫杉醇的可持续生产方法,例如以紫杉烷类晚期中间体为原料的半合成法,以及植物细胞培养合成法(图 1)。本文专栏 1 归纳了现有的紫杉醇生产策略,并强调:为保障紫杉醇的稳定供应、同时保护生态系统,亟需建立可持续的生产平台。
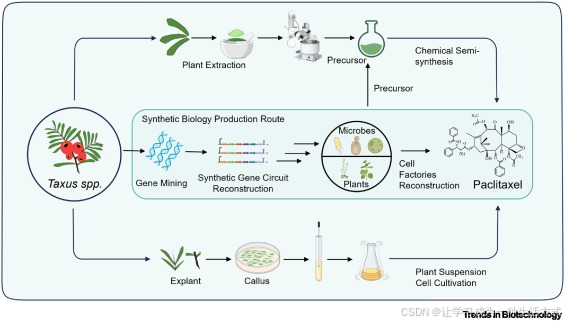
图 1 植物源抗癌药物紫杉醇的生产策略示意图
当前紫杉醇的生产方法包括从红豆杉属植物或红豆杉悬浮细胞培养物中提取关键前体,再通过半合成工艺制备紫杉醇。此外,将紫杉醇生物合成酶在微生物或植物源宿主系统中进行异源表达,也可实现紫杉醇关键前体或相关紫杉烷中间体的合成。
专栏 1 紫杉醇的多元生产来源及其可持续供应的局限性
科研人员已围绕紫杉醇生产开展了大量探索,涵盖化学全合成、半合成、植物细胞培养,以及利用宿主相关的工程化内生真菌(如安氏紫杉菌)进行生物合成等技术路径 [4,5]。但海尼希(Heinig)团队的研究证实,包括曾被认为具备合成能力的安氏紫杉菌在内,所有内生真菌均不具备紫杉醇的从头合成能力;这些真菌体内检测到的微量紫杉醇,实则是从宿主红豆杉植株中累积的残留成分 [6]。施塔德勒(Stadler)团队的研究进一步否定了工程化内生真菌作为紫杉醇生产体系的可行性,指出早期研究的误判源于检测方法的缺陷(如交叉反应免疫分析),并证实这类内生真菌无法维持紫杉醇的持续合成 [7]。尽管化学全合成技术已突破紫杉醇生产的多项技术壁垒,但该方法仍受限于合成路线冗长、反应步骤复杂、产物收率低及生产成本高昂等问题,难以实现规模化商业化生产。红豆杉悬浮细胞的大规模培养技术已取得显著产业化突破,例如全球生物技术龙头企业法顿生物科技公司,便成功实现了红豆杉悬浮细胞的规模化培养,达成紫杉醇的商业化量产。目前,半化学合成法仍是紫杉醇的主流生产手段,该方法以从红豆杉植株或培养的红豆杉细胞中提取的关键中间体(如巴卡亭 III、10 - 去乙酰巴卡亭 III)为底物 [8]。然而,此方法仍需依赖野生红豆杉资源,无法从根本上解决紫杉醇的可持续供应难题与合成成本高企的问题。
合成生物学(详见术语表)为紫杉醇、长春碱等高附加值天然产物的生产提供了极具潜力的策略 [9]。近年来,在红豆杉基因组测序及紫杉醇关键前体巴卡亭 III的生物合成途径解析方面已取得突破性进展 [10,11]。蒋氏团队近期鉴定出该途径中缺失的关键酶类,包括紫杉烷 - 9α- 羟化酶(T9αH)与紫杉烷氧杂环丁烷合成酶 1(TOT1),从而推动了巴卡亭 III 的全生物合成 [12]。此外,梁氏团队详细阐明了将巴卡亭 III 转化为紫杉醇的最后两步酶促修饰反应 ——C2′α- 羟基化反应与3′-N - 苯甲酰化反应[1]。麦克卢恩(McClune)团队首创了单细胞核测序与 CRISPR 基因扰动联用技术(mpXsn),通过该技术解析了红豆杉的基因调控网络 [13]。研究发现,一种类核转运因子 2 蛋白FoTO1可与 ** 紫杉二烯 5α- 羟化酶(T5αH)和紫杉二烯合成酶(TXS)** 形成蛋白复合体,使紫杉醇早期合成途径的产物收率提升 10-17 倍。结构建模分析表明,FoTO1 蛋白发挥分子支架作用,通过与 TXS 和 T5αH 的相互作用,稳定酶 - 底物复合物结构,保障催化反应的有序进行,同时减少非靶向氧化副产物的生成。该发现为异源紫杉醇合成中靶向人工酶支架的设计提供了重要理论依据。
尽管如此,在异源微生物中重构紫杉醇完整合成途径仍是一项重大挑战。该途径包含约 19 步紫杉烷生物合成酶促反应,其中近 50% 的反应由细胞色素 P450 酶催化,而这类酶的催化机制尚未被完全阐明 [2,11,14]。目前,紫杉醇早期关键前体紫杉二烯的克级合成已实现,但下游合成途径的重构仍受限于多重瓶颈:P450 酶固有催化效率低下、与异源宿主的适配性差,以及核心酶催化过程中副产物大量生成等。这些问题导致代谢流严重分流,进而严重制约了紫杉醇前体的从头生物合成效率。
近年来已有多篇综述总结了紫杉醇生物合成机制的解析进展 [15,16],为该领域研究提供了重要参考。本研究聚焦于紫杉醇前体可持续生产的核心挑战,并提出一系列前沿合成生物学策略以攻克这些难题。具体而言,我们系统剖析了 P450 酶底物宽泛性、代谢流失衡等关键瓶颈,并针对性地提出解决方案,包括:构建以藻类、非常规酵母及丝状真菌为代表的新型底盘细胞系统,提升植物源 P450 酶的异源适配性;开发整合无细胞合成与化学酶法的杂合合成技术;利用 FoTO1 等调控因子,减少 T5αH 等 P450 酶的副产物生成;以及应用机器学习驱动的途径优化技术与人工合成微生物菌群策略。上述策略共同构建了紫杉醇前体及其他复杂植物源天然产物规模化生产的技术路线图。
紫杉醇生物合成途径的解析
紫杉醇的生物合成途径已通过生物化学与部分遗传学手段得到解析,该途径可分为三个阶段:以香叶基香叶基焦磷酸(GGPP)为起始底物合成紫杉二烯 - 5α- 醇;将紫杉二烯 - 5α- 醇转化为巴卡亭 III(详见专栏 2);以及苯异丝氨酸与巴卡亭 III 结合,最终生成紫杉醇(详见专栏 3)。
紫杉醇生物合成的首个定向步骤是生成 C20 萜类化合物紫杉二烯,该反应由位于质体中的紫杉二烯合成酶(TXS)催化,以 GGPP 为底物 [12,23]。克罗托(Croteau)团队为紫杉醇生物合成途径的解析奠定了重要基础,其研究证实紫杉二烯是紫杉烷骨架合成的首个关键中间体,并完成了该反应的催化酶 TXS 的分离纯化与功能鉴定 [24]。紫杉二烯生成后,需经过一系列修饰反应转化为紫杉醇关键前体巴卡亭 III,这些修饰反应包括酶促羟基化、酰基化、酮基化及氧杂环丁烷环的形成(见图 2)。近期研究已鉴定出多个紫杉醇合成必需的新型酶类,例如紫杉烷 C4β-C20 环氧化酶、紫杉烷 - 1β- 羟化酶(T1βH)、紫杉烷 - 9α- 羟化酶(T9αH)及紫杉烷 9α- 双加氧酶[18]。
专栏 2 巴卡亭 III 紫杉烷骨架的合成:核心途径与关键反应
紫杉醇的生物合成始于植物二萜类化合物的通用前体香叶基香叶基焦磷酸(GGPP)。GGPP 由 1 分子二甲基烯丙基焦磷酸(DMAPP)与 3 分子异戊烯基焦磷酸(IPP)在香叶基香叶基焦磷酸合成酶(GGPPS)催化下缩合生成。在植物细胞内,IPP 与 DMAPP 通过两条内源途径合成:细胞质中的甲羟戊酸途径(MVA)与叶绿体中的甲基赤藓糖醇磷酸途径(MEP)[12]。IPP 与 DMAPP 可在 ** 异戊烯基焦磷酸异构酶(IDI)** 的作用下相互转化。随后,GGPPS 催化 IPP 与 DMAPP 缩合生成 GGPP;TXS 进一步催化 GGPP 环化反应,主要生成紫杉二烯 [紫杉 - 4 (5),11 (12)- 二烯](约占 95%),同时伴随少量异紫杉二烯 [紫杉 - 4 (20),11 (12)- 二烯] 的生成 [17]。
巴卡亭 III 的合成需经过一系列酶促修饰反应,包括羟基化、羟基酰基化、酮基化及氧杂环丁烷环的形成。其中,紫杉二烯 C5 位的羟基化反应是该阶段的起始步骤,由紫杉二烯 - 5α- 羟化酶(CYP725A4,T5αH)催化,生成紫杉醇合成途径中的首个羟基化中间体紫杉 - 4 (5),11 (12)- 二烯 - 5α- 醇(紫杉二烯 - 5α- 醇),同时伴随多种紫杉烷单氧及双氧化副产物的生成(如5 (12)- 氧杂 - 3 (11)- 环紫杉烷(OCT)与5 (11)- 氧杂 - 3 (11)- 环紫杉烷(异 OCT))。当异紫杉二烯作为底物时,可被 T5αH 直接羟基化生成紫杉二烯 - 5α- 醇。
紫杉二烯 - 5α- 醇后续存在两条分支代谢途径:(1)紫杉二烯醇 - 5α-O - 乙酰转移酶(TAT)催化其 C5α 羟基发生乙酰化反应,生成紫杉 - 4 (20),11 (12)- 二烯 - 5α- 乙酸酯,该产物经紫杉烷 - 10β- 羟化酶(T10βH)催化羟基化,生成紫杉 - 4 (20),11 (12)- 二烯 - 5α,10β- 二醇 - 5 - 乙酸酯;(2)紫杉烷 - 13α- 羟化酶(T13αH)催化紫杉二烯 - 5α- 醇的 C13 位羟基化,生成紫杉 - 4 (20),11 (12)- 二烯 - 5α,13α- 二醇,该产物再依次经过 C5α 乙酰化与 C10β 羟基化反应,生成紫杉二烯 - 5α,10β,13α- 三醇 - 5 - 乙酸酯。
此后,该中间体的 C1、C2、C7、C9 位将发生多轮酶促羟基化反应,同时伴随 C9 位氧化及氧杂环丁烷环的形成 [2,18]。紫杉烷 - 2α-O - 苯甲酰转移酶(TBT)进一步催化 2 - 去苯甲酰基紫杉烷转化为主要中间体10 - 去乙酰巴卡亭 III(10-DAB);随后,10 - 去乙酰巴卡亭 III-10-O - 乙酰转移酶(DBAT)催化 10-DAB 的 C10 位羟基乙酰化,生成紫杉醇的核心骨架中间体巴卡亭 III[19]。
上述紫杉烷骨架修饰反应主要由细胞色素 P450 酶介导的羟基化反应与酰基转移酶介导的乙酰化反应组成,但这些反应的精确顺序尚未明确 [13,20]。值得注意的是,紫杉醇的生物合成并非单一的线性途径,而是存在多个分支节点,进而形成结构高度多样化的紫杉烷类化合物 [12]。
专栏 3 巴卡亭 III 的后修饰与紫杉醇的生成
紫杉醇的 C13 侧链是其抗癌活性的关键结构基础,该侧链的生物合成主要包括两步反应:酶促异构化与酯化反应 [1]。该途径的起始步骤为:苯丙氨酸氨基变位酶(PAM)催化L - 苯丙氨酸发生异构化反应,生成β- 苯丙氨酸;随后,β- 苯丙氨酸 - CoA 连接酶(PCL)催化 β- 苯丙氨酸发生酯化反应,生成活化形式的β- 苯丙氨酸 - CoA。
下一步,3 - 氨基 - 13 - 苯丙酰转移酶(BAPT)以 β- 苯丙氨酸 - CoA 为酰基供体,催化巴卡亭 III 的 C13 位发生酰基化反应,生成β- 苯丙酰基巴卡亭 III。紧接着,紫杉烷 - 2′α- 羟化酶(T2α′H)催化 β- 苯丙酰基巴卡亭 III 侧链的 C2′位羟基化,生成中间体3′-N - 去苯甲酰基紫杉醇[21]。最终,**3′-N - 去苯甲酰基 - 2′- 脱氧紫杉醇 - N - 苯甲酰转移酶(DBTNBT)** 催化 3′-N - 去苯甲酰基紫杉醇侧链 C3′位的 N - 苯甲酰化反应,从而生成紫杉醇 [22]。
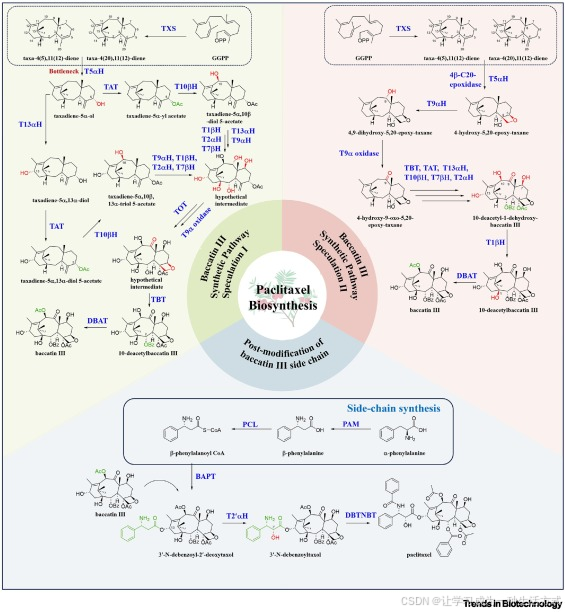
图 2 紫杉醇生物合成途径示意图
图中黄绿模块展示了合成巴卡亭 III 的一条推测生物合成途径,粉色模块代表另一条备选合成途径,灰色模块则表示 β- 苯异丝氨酸侧链的合成及与巴卡亭 III 偶联的后修饰途径。
缩写注释TXS:紫杉二烯合成酶;T5αH:紫杉二烯 - 5α- 羟化酶;TAT:紫杉二烯 - 5α- 醇 - O - 乙酰转移酶;T10βH:紫杉烷 - 10β- 羟化酶;T13αH:紫杉烷 - 13α- 羟化酶;T2αH:紫杉烷 - 2α- 羟化酶;T9αH:紫杉烷 - 9α- 羟化酶;T7βH:紫杉烷 - 7β- 羟化酶;T1βH:紫杉烷 - 1β- 羟化酶;TBT:紫杉烷 - 2α-O - 苯甲酰转移酶;DBAT:10 - 去乙酰巴卡亭 III-10-O - 乙酰转移酶;TOT:紫杉烷氧杂环丁烷合成酶;BAPT:巴卡亭 III-3 - 氨基 - 13 - 苯丙酰转移酶;T2′αOH:紫杉烷 - 2′α- 羟化酶;DBTNBT:3′-N - 去苯甲酰基 - 2′- 脱氧紫杉醇 - N - 苯甲酰转移酶;PAM:苯丙氨酸氨基变位酶;PCL:β- 苯丙氨酸 - CoA 连接酶。
氧杂环丁烷环是由 1 个氧原子和 3 个碳原子构成的四元杂环,是紫杉醇独有的结构特征,同时也是其抗癌活性的关键所在。近年来的研究加深了人们对氧杂环丁烷环形成的酶促机制的理解。2023 年,张氏团队发现了一种新型C4β-C20 环氧化酶,该酶属于 α- 酮戊二酸 / 亚铁离子依赖性双加氧酶,可催化 C4β-C20 氧杂环丁烷环的形成 [18]。但由于难以分离得到足量的环氧化产物用于核磁共振波谱(NMR)结构鉴定,该反应的精确机制目前仍停留在推测阶段。2024 年,赵氏团队证实,此前已被鉴定为紫杉二烯 - 5α- 羟化酶的CYP725A4(细胞色素 P450 家族 725 亚家族 A 成员),可催化紫杉二烯的多位点氧化反应,且该反应可能通过两步环氧化机制形成氧杂环丁烷环 [17]。
与此同时,蒋氏团队利用本氏烟草底盘系统对候选基因开展酶活测定,鉴定出一种兼具双重功能的 P450 酶 ——TOT1,该酶参与氧杂环丁烷环的生物合成。此外,蒋氏团队还发现,在红豆杉细胞中敲低TOT1基因的表达后,巴卡亭 III 与紫杉醇的生物合成量均显著下降 [12]。杨氏团队报道了一种功能类似的 P450 酶CYP725A55,其可通过级联氧化反应伴随酰基重排,催化氧杂环丁烷环的形成 [20]。另外,李氏团队从南方红豆杉中分离得到一种细胞色素 P450 酶TmCYP1,该酶同样具备催化氧杂环丁烷环形成的功能。研究人员探究了 TmCYP1 的催化机制,推测其通过 Δ⁴ˏ²⁰双键与 C5-OAc 基团之间的氧化 - 重排反应发挥作用,氧杂环丁烷环的形成可能为协同反应过程 [25]。上述研究成果共同深化了人们对氧杂环丁烷环形成机制及植物源 P450 酶催化多样性的认知。
复杂异源途径的重构、整合与优化
在异源宿主中重构并优化紫杉醇生物合成途径,对于紫杉烷类化合物的生产而言,面临着三个相互关联的核心挑战。其一,前体物质(如 GGPP)的供应需与下游限速酶的催化能力实现精准平衡;其二,植物源 P450 酶在微生物宿主中的催化效率固有偏低,这主要源于其功能表达效率差、辅因子适配性不足以及膜整合效果欠佳;其三,紫杉醇合成途径的代谢流,会与宿主自身关键途径争夺还原型烟酰胺腺嘌呤二核苷酸磷酸(NADPH)与碳源,这使得紫杉烷产量与宿主细胞活性之间形成难以调和的权衡关系 [26,27,28]。
微生物合成小白菊内酯的研究经验表明,靶向性补充 NADPH 与扩增内质网(ER)可协同提升 P450 酶的功能活性 [29]。当前主流的优化策略 —— 前体途径改造、酶分子工程、CRISPR/RNAi 介导的代谢流调控、人工合成微生物菌群构建以及杂合合成系统开发 —— 均致力于协调紫杉醇生产与宿主生理代谢的适配性(见图 3)。
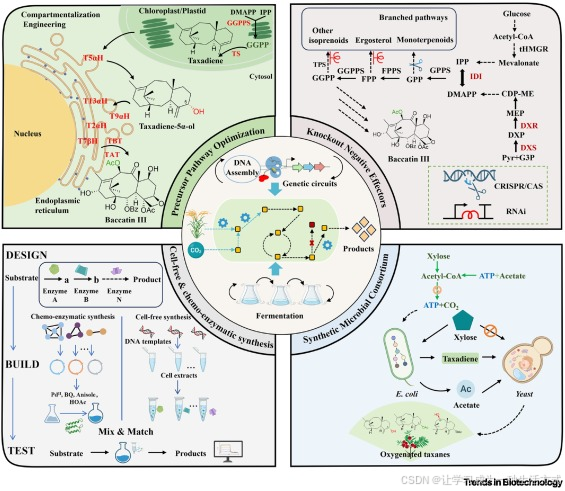
图 3 紫杉烷生物合成的多元化合成生物学策略示意图
多种代谢工程策略已被成功应用于重定向代谢流,使其向紫杉烷生物合成方向倾斜。这些策略包括提升紫杉烷前体供应能力、对紫杉烷相关代谢途径实施可调式调控、构建无细胞生化合成体系,以及人工合成微生物菌群。此外,基于 CRISPR 与 RNAi 技术的靶向基因表达调控及代谢网络重构策略,在突破紫杉烷从头生物合成途径瓶颈方面发挥着关键作用。已有研究表明,内质网(ER)网络可延伸至叶绿体内部,这与近期在植物萜类化合物合成过程中观察到的内质网 - 叶绿体物理耦合现象相吻合 [30]。化学 - 生物耦合反应体系说明:PdⅡ 代表醋酸钯,BQ 代表对苯醌。
缩写注释CRISPR:成簇规律间隔短回文重复序列;ER:内质网。
前体供应优化与正向调控因子过表达
稳定的前体供应是实现高效紫杉烷合成的必要条件,但单纯提高前体水平并不足以提升产量;其增效作用的发挥,还依赖于对下游酶的活性调控,从而实现代谢流的精准分配,避免出现代谢流分流、副产物累积或中间代谢物毒性等问题。在紫杉醇生物合成途径中,异戊烯基焦磷酸(IPP)与二甲基烯丙基焦磷酸(DMAPP)是萜类化合物合成的通用前体,二者分别来源于细胞质中的甲羟戊酸(MVA)途径和质体中的甲基赤藓糖醇磷酸(MEP)途径。对这两条途径的优化已成功提高紫杉烷的产量 [5,31]。例如,引入异源 MVA 途径或优化内源 MEP 途径,均可显著提升紫杉烷的滴度,但这类改良需与酶工程技术协同进行,以减少副产物生成;否则,过量的前体物质将造成大量代谢浪费。值得注意的是,紫杉二烯合成酶(TXS)与紫杉二烯 - 5α- 羟化酶(T5αH)的底物宽泛性,是紫杉醇生物合成过程中的又一关键瓶颈。为攻克这一难题,基于结构的酶分子工程技术已成为行之有效的解决方案(详见专栏 4)。通过定点突变,可使异紫杉二烯(一种主要副产物)的生成量降低 10%–30%,并将代谢流更多地导向目标产物紫杉二烯。
专栏 4 紫杉醇生物合成限速酶(TXS 与 T5αH)的分子改造
紫杉二烯合成酶(TXS)是紫杉醇生物合成途径中的首个专用萜类环化酶,负责催化关键的环化反应,将香叶基香叶基焦磷酸(GGPP)转化为主要产物紫杉 - 4 (5),11 (12)- 二烯 [5]。天然 TXS 酶由 862 个氨基酸组成,其 N 端含有一段约 80 个氨基酸残基的叶绿体转运肽(CTP),该结构可引导酶蛋白在植物细胞内定位于质体 [32,33]。值得关注的是,去除该转运肽后得到的TXS 伪成熟体,在异源宿主中的催化效率与稳定性均显著提升 —— 这一点已在大肠杆菌异源表达体系中得到验证 [5]。此外,关键酶(如 TXS、T5αH)的底物宽泛性及辅因子可利用性限制,也是导致其催化效率偏低的重要原因。克萨尔(Köksal)团队通过对截短型 TXS 酶的晶体学研究,阐明了该酶催化效率提升的结构基础:其特有的三结构域 α- 螺旋构象,能够有效促进底物结合与催化反应的进行 [33]。何氏团队的研究则进一步揭示了 TXS 酶的催化机制,鉴定出酶活性中心中调控完整催化循环的关键氨基酸残基 —— 该循环涵盖底物离子化、碳正离子稳定化及最终环化反应等多个步骤 [34]。TXS 酶同样存在底物宽泛性问题,其在生成主产物紫杉二烯的同时,会伴随约 5% 的副产物异紫杉二烯生成。通过对 TXS 酶特定氨基酸残基(如 V584、Q609、Y688、Y762、Q770 及 F834)进行定点突变,可将其底物宽泛性降低 10%–25%,从而进一步提升目标产物紫杉二烯的代谢流占比 [34]。该研究还鉴定出若干与紫杉烷类副产物生成相关的活性中心残基。此外,埃德加(Edgar)团队的研究证实,定点突变介导的 TXS 酶分子改造,是提升产物选择性的有效手段 [35]。通过改造,他们成功将另一种环化产物紫杉 - 4 (20),11 (12)- 二烯的产量与选择性提升至原来的 2.4 倍。综上,这些研究深化了人们对 TXS 酶功能机制的认知,并为其在紫杉醇异源生物合成中的应用奠定了基础。
30 余年来,在异源系统中重构紫杉醇生物合成早期步骤的核心瓶颈,一直是紫杉醇合成相关细胞色素 P450 酶的功能性表达难题 [17]。紫杉二烯 - 5α- 羟化酶(T5αH)负责催化紫杉醇生物合成的第一步羟基化反应,但其底物宽泛性较高,催化过程中会生成多种紫杉二烯氧化副产物 [19]。而在这些产物中,仅有紫杉二烯 - 5α- 醇是紫杉醇合成的直接前体,其余副产物均会导致代谢流偏离目标途径。T5αH 酶的高底物宽泛性与低催化活性,严重阻碍了紫杉醇在微生物异源系统中的从头生物合成进程 [5,14,36]。自 1996 年首次从红豆杉属植物中鉴定出 T5αH 酶以来,该酶便成为 P450 酶分子工程的核心研究靶点。研究人员已探索出多种改造策略,包括 N 端修饰、P450 电子传递链优化、核糖体介导的表达调控及亚细胞区室化定位等。同时,针对催化温度、氧浓度、pH 值及辅因子(如 NADPH)可利用性等关键反应条件的优化工作也已全面开展 [5,14,19,37,38]。例如,比格斯(Biggs)团队通过 N 端修饰,在大肠杆菌中实现了 T5αH 酶及其伴侣蛋白 P450 还原酶(CPR)的高效表达,使氧化型紫杉烷的滴度提升 5 倍,达到 570 mg/L±45 mg/L [37]。尽管取得上述进展,人们对 T5αH 酶详细催化机制的认知仍未取得突破性进展。亚达夫(Yadav)团队基于 6 种 P450 酶的晶体结构,构建了 T5αH 酶的同源建模结构,并设计出 53 种突变体,其中仅 6 种突变体表现出转化率提升及紫杉二烯 - 5α- 醇选择性增强的特性 [38]。2024 年,刘氏团队尝试利用多种表达宿主对 T5αH 酶进行异源功能鉴定,结果发现所有测试宿主均存在过度氧化副产物生成的问题。通过调控 T5αH 酶表达启动子的活性,他们成功降低了副产物水平,同时使紫杉二烯 - 5α- 醇的累积量提升 3 倍 [19]。此外,宋氏团队结合 X 射线晶体学、分子动力学(MD)模拟、量子力学 / 分子力学(QM/MM)联用计算及独立量子力学(QM)计算等技术,解析了 CYP725A4 - 紫杉二烯酶 - 底物复合物的晶体结构 [39]。该研究揭示了 CYP725A4 酶的详细催化机制,为后续 T5αH 酶的分子改造工作奠定了理论基础。未来的研究应聚焦于攻克异源表达适配性难题,以提升流向紫杉二烯 - 5α- 醇的代谢流占比,并降低因多种紫杉烷氧化副产物导致的产物分离复杂性。
紫杉烷合成与宿主生物量积累之间的中心碳代谢物竞争,是紫杉醇异源合成面临的另一挑战。** 异戊烯醇利用途径(IUP)** 为解决这一问题提供了新思路:该途径可以外源异戊烯醇或异戊二烯醇为底物,正交合成 IPP/DMAPP,从而使紫杉醇前体的供应与宿主内源代谢途径解耦 [41]。例如,在酿酒酵母中引入 IUP 途径后,IPP/DMAPP 的库容量较内源途径提升 147 倍 [42];而体外 IUP 系统的紫杉二烯产量,也达到传统细胞合成体系的 3 倍 [41]。与步骤繁琐、辅因子需求高的 MEP/MVA 途径不同,IUP 途径的优化更为简便 —— 该途径仅需两步酶促反应,且仅依赖单一辅因子(ATP)。尤为关键的是,IUP 途径的代谢正交性可有效避免目标合成途径与宿主中心代谢途径之间的碳源竞争,从而保障宿主细胞的活性。
基于 CRISPR 与 RNAi 技术的负向调控因子敲除 / 敲低
竞争性代谢途径会分流紫杉醇合成的碳源代谢流,进而显著降低紫杉烷产量。为解决这一问题,基于 CRISPR 的基因编辑技术与 RNAi 技术,已成为阻断或弱化竞争性途径、将碳源代谢流重定向至目标紫杉烷合成的可行策略(见表 1)。在酿酒酵母中,利用 CRISPR 技术沉默固醇合成途径中的关键基因ERG9(编码角鲨烯合成酶),可将萜类前体从固醇合成途径导向紫杉烷合成途径,使紫杉二烯产量提升 1 倍 [60,61]。在另一项研究中,科研人员将酵母内源ERG9基因的启动子替换为弱启动子变体,并结合前体 “推拉” 策略,协同将紫杉二烯的代谢流提升至原来的 2 倍 [53]。这些结果表明,CRISPR 介导的竞争性途径沉默,与其他技术手段联用,可通过减少碳源分流显著提升紫杉烷产量。类似地,CRISPR 介导的 DNA 甲基化技术,是调控红豆杉细胞中苯丙烷途径代谢流的有效手段。该途径不仅为紫杉醇合成提供苯丙氨酸衍生物前体,同时还参与木质素合成等宿主必需的生理过程 [62]。牛顿(Newton)团队利用 CRISPR 介导的 DNA 甲基化技术,敲低了苯丙烷途径中的首个专用酶 —— 苯丙氨酸解氨酶(PAL)的表达水平,而该酶正是紫杉醇侧链合成所需苯丙氨酸衍生物的供给来源。此次敲低使紫杉醇的累积量显著提升 25 倍 [62]。研究人员还采用化学抑制剂对苯丙烷途径的下游环节进行抑制,并结合外源苯丙氨酸饲喂策略,二者协同作用进一步提高了紫杉醇的生物合成效率。
Table 1. Heterologous expression systems for taxane production
|
Empty Cell |
Host |
Product |
Titer |
Strategy |
Key advantages and limitations of wild-type chassis |
Date |
Refs |
|
1 |
Escherichia coli |
Taxadiene |
1.3 mg/l |
Overexpression of IDI, GGPPS, TXS, and DXP genes |
Advantages: |
2001 |
|
|
200 mg/l |
Expressing the MEP pathway genes under the control of the T7 promoter, regulating the downstream pathway using the T7, Trc, and T5 promoters, optimizing culture temperature to 22°C |
Rapid growth; mature Genetic manipulation tools; clear genetic background; native MEP pathway for isoprenoid precursor synthesis; high fermentation scalability in industrial settings. |
2012 |
||||
|
93.5 mg/l |
Constructing a fusion protein of TXS and GGPPS and increasing the expression of the rate-limiting enzymes DXS and IDI in MEP |
2022 |
|||||
|
1 g/l |
A multivariate modular approach to metabolic pathway engineering |
2010 |
|||||
|
Taxadiene-5α-ol |
7 mg/l |
Introduction of TbrTXS, Taxus CPR, T5αOH-GSTGS-CPR, and a heterologous MVA pathway; optimization of culture conditions |
2022 |
||||
|
58 ± 3 mg/l |
Introduction of TXS and T5αH in a multivariate modular E. coli system |
2010 |
[5] |
||||
|
Oxygenated taxanes |
27 mg/l |
Introduction of a heterologous MVA pathway and expressing TbrTXS, Taxus CPR, T5αH-GSTGS-CPR models |
2022 |
[31] |
|||
|
570 ± 45 mg/l |
Optimizing P450 expression, reductase partner interactions, and N-terminal modifications |
2016 |
|||||
|
Limitations: |
|||||||
|
Prokaryotic system (lacks eukaryotic protein folding machinery); without ER (critical for P450 activity); not GRAS certified. |
|||||||
|
2 |
Saccharomyces cerevisiae |
Taxadiene |
8.7 mg/l |
Coexpression of tHMGR, mutant regulatory protein UPC2-1, GGPPS and TXS, codon optimized T. chinensis TXS |
Advantages: |
2008 |
|
|
72.8 mg/l |
Construction of a yeast cell factory with different GGPPSs guided by computer-aided protein modeling, overexpression ERG20 and tHMGR and TXS gene |
Eukaryotic system (ER for P450 folding and activity); native MVA pathway for isoprenoid synthesis; GRAS certified; mature genetic tools (e.g., CRISPR, YeastFab); robust to industrial fermentation conditions (e.g., low pH, high density). |
2014 |
||||
|
129 mg/l |
Multicopy chromosomal integration of TXS with a combination of fusion protein tags |
2020 |
|||||
|
215 mg/l |
Using in silico design algorithms and wet-lab screening |
2023 |
|||||
|
Oxygenated taxanes |
33 mg/l |
A mutualistic E. coli and S. cerevisiae consortium for the production of oxygenated taxanes |
2015 |
||||
|
78 mg/l |
High-throughput microscale optimization, improvement of fermentation process |
2021 |
|||||
|
361.4 ± 52.4 mg/l |
Promoter pHXT7, fusion expression of T5αH and CPR, resting cell assays with optimal neutral pH |
2022 |
|||||
|
Taxadiene-5α-ol |
20 mg/l |
Optimizing the biosynthesis of oxygenated and acetylated paclitaxel precursors using advanced bioprocessing strategies |
2021 |
[50] |
|||
|
38.1 ± 8.4 mg/l |
Using a low-glucose inducible promoter pHXT7; fusion expression of T5αH and CPR; assayed the production using resting cells in neutral pH |
2022 |
[51] |
||||
|
42 mg/l |
Overcoming nutritional stress-induced pseudohyphal growth, coupling a statistical definitive screening design approach with the high-throughput microbioreactors |
2022 |
|||||
|
43.65 mg/l |
Computational metabolic engineering and genome-scale modeling strategy |
2023 |
[49] |
||||
|
Taxadien-5α-yl-acetate |
3.7 mg/l |
Improvement of fermentation process, e.g., pH optimization |
2021 |
[50] |
|||
|
22 mg/l |
Using a high-throughput microbioreactor and a statistical deterministic screening strategy |
2022 |
[52] |
||||
|
Taxadien-5α-acetate |
26.2 mg/l |
A combinatorial in silico system biology approach |
2023 |
[49] |
|||
|
Paclitaxel |
0.97 μg/l |
Reconstruct the late pathway in yeast and synthesize paclitaxel from baccatin III |
2025 |
||||
|
Limitations: |
|||||||
|
No native MEP pathway (relies solely on MVA pathway); native sterol synthesis pathway competes for FPP/GGPP precursors; slower growth than prokaryotes. |
|||||||
|
Yarrowia lipolytica |
Taxadiene |
101.4 mg/l |
A ‘push–pull’ strategy, fusion expression of five solubilizing tags and TXS, a multicopy iterative integration |
Advantages: |
2023 |
||
|
High tolerance to harsh conditions; strong lipid metabolism (supporting terpenoid precursor supply). |
|||||||
|
Limitations: |
|||||||
|
Fewer mature genetic tools than S. cerevisiae; native metabolic flux tends toward lipid synthesis |
|||||||
|
3 |
Nicotiana benthamiana |
Taxadiene |
11-27 μg/g DW |
Ectopic expression of the TXS gene and elicitor treatment or metabolic pathway shunting of the terpenoid pathway |
Advantages: |
2014 |
|
|
56.6 ± 3.2 μg/g fresh weight |
A chloroplastic compartmentalized metabolic engineering strategy, coexpression of DXS and GGPPS |
Native plant chassis (MEP/MVA dual pathways for isoprenoids); inherent P450 folding/co-factor matching system (ideal for plant-derived P450s); transient expression capability (fast gene function verification). |
2019 |
||||
|
Taxadiene-5α-ol |
1.3 ± 0.5 μg/g FW |
A chloroplastic compartmentalized metabolic engineering strategy, combined with the enhancement of isoprenoid precursor |
2019 |
[14] |
|||
|
5α,10β-diacetoxytaxadien-13α-ol |
63 μg/g DW |
Reconstitution of an early paclitaxel biosynthetic network in host involving TXS, T5αH, TAT, T10βH, DBAT, and T13αΗ |
2024 |
||||
|
Paclitaxel |
64.29 ng/g FW |
Transient expression of PCL with BAPT, PAM, DBTNBT, T2’OH |
2023 |
||||
|
Baccatin III |
154.87 ng/g FW |
Transient expression of C4β-C20 cyclooxygenase, T9αOH, T1βOH, and T9OX with nine other known genes |
2023 |
[18] |
|||
|
~50 ng/g |
Transient expression of TOT and T9αH-1 with seven other known synthetic genes |
2024 |
|||||
|
10-30 μg/g DW |
Multiplexed perturbation × single nuclei (mpXsn), overexpression nuclear transport factor two (NTF2)-like protein, FoTO1 |
2025 |
|||||
|
Nicotiana tabacum |
Taxadiene |
87.8 μg/g DW |
Expressing TXS with a chloroplast transit peptide |
2021 |
|||
|
Arabidopsis thaliana |
Taxadiene |
600 ng/g DW |
Transgene expression using a glucocorticoid-mediated system |
2004 |
|||
|
Limitations: |
|||||||
|
Long growth cycle; low biomass density in suspension culture; high cost of large-scale cultivation than microorganism; unstable productivity in long-term culture. |
|||||||
|
4 |
Alternaria alternata TPF6 |
Taxadiene |
61.9 ± 6.3 μg/l |
Co-overexpression of IDI, tHMGR and TXS in filamentous fungi |
Advantages: |
2017 |
|
|
Eukaryotic filamentous fungus (possessing ER for partial P450 folding); native MVA pathway; potential for solid-state fermentation. |
|||||||
|
Limitations: |
|||||||
|
Not GRAS certified; complex mycelial growth (hard to control in liquid fermentation); few genetic manipulation tools; slow growth. |
|||||||
|
5 |
Bacillus subtilis |
Taxadiene |
17.8 mg/l |
Overexpression of the MEP pathway, GGPPS, TXS gene |
Advantages: |
2019 |
|
|
GRAS certified; robust to environmental stress; clear genetic background; native MEP pathway; capability for protein secretion. |
|||||||
|
Limitations: |
|||||||
|
Prokaryotic system (without P450 folding machinery/ER); without native MVA pathway; lower isoprenoid precursor flux than E. coli. |
|||||||
|
6 |
Synechocystis sp. PCC 6803 |
Taxadiene-5α-ol |
4.32 mg/l |
Coexpression of heterologous GGPPS and TXS in a high-density cultivation culture system and membrane-mediated CO2 supply |
Advantages: |
2024 |
|
|
Photoautotrophic (CO₂ and solar energy as carbon/energy source); native MEP pathway; thylakoid membranes (support partial P450 activity); low culture cost. |
|||||||
|
Limitations: |
|||||||
|
Slow growth than E. coli; without native MVA pathway. |
除 CRISPR 外的调控策略:微小 RNA 介导的紫杉醇生物合成优化
除 CRISPR 技术外,微小 RNA(miRNA)介导的调控策略也为紫杉醇生物合成优化提供了可行方案。近期研究表明,内皮细胞特异性的 miR858b-MYB1L 调控模块在南方红豆杉紫杉醇生物合成过程中发挥核心作用。具体而言,miR858b 可靶向作用于转录因子基因MYB1L,而该转录因子能够激活紫杉醇生物合成途径中的两个关键基因:紫杉烷 - 2α-O - 苯甲酰转移酶基因(TBT)与巴卡亭 III-3 - 氨基 - 13 - 苯丙酰转移酶基因(BAPT)[63]。该 miR858b-MYB1L 模块通过精准调控红豆杉根、茎内皮细胞中TBT与BAPT的表达水平,在紫杉醇生物合成的转录调控网络中扮演关键角色。
基于基因线路的代谢途径组分可调式调控
紫杉醇的生物合成是一个包含 19 步酶促反应的级联过程,其固有复杂性要求对该途径进行精准调控,以避免代谢流失衡引发的中间产物毒性积累或产物产量下降 [61,64-66]。合成基因线路可通过可编程的、配体响应性调控,为这一问题提供高效解决方案。基于生物传感器的动态调控技术,能够在代谢物浓度波动与酶表达水平调节之间建立实时反馈环路。该调控模式的核心是代谢物响应型生物传感器(基因线路的核心元件),其可感知输入信号(即代谢物浓度变化)并输出调控酶表达的信号。这种策略在萜类化合物合成途径中成效显著:例如,在酿酒酵母中构建的法尼基焦磷酸(FPP)响应型基因线路,不仅有效缓解了 FPP 诱导的细胞毒性,还使无环倍半萜(紫穗槐二烯)的产量提升 1 倍。这一成果对紫杉醇生物合成研究具有重要参考价值,因为二者均依赖萜类前体物质 [67]。在另一项研究中,科研人员利用来源于谷氨酸棒杆菌的转录调控蛋白CrtR与PcrtE-gfpuv融合报告基因,构建了基因编码型 GGPP 生物传感器,并验证了该传感器可将荧光信号强度与细胞内 GGPP 浓度相关联 [68]。以上两例经过验证的生物传感器应用案例,证明了利用生物传感器优化萜类衍生物合成代谢流的可行性,为其在紫杉醇生物合成研究中的应用奠定了关键基础。
代谢网络重构是提升紫杉烷产量的另一重要策略,该策略可实现对紫杉烷相关代谢途径的靶向精准调控 [69,70]。具体包含四项核心技术:细胞器区室化、人工蛋白支架、蛋白融合与转录因子介导的调控。细胞器区室化策略通过对异源代谢途径组分进行靶向定位优化,提高局部底物浓度,同时降低中间代谢物的细胞毒性。例如,研究人员将 TXS、T5αH 及细胞色素 P450 还原酶(CPR)靶向定位到本氏烟草的叶绿体中,使紫杉二烯的产量提升最高达 1 倍 [14]。与之类似,在工程化酿酒酵母中表达香叶基香叶基焦磷酸合成酶 - 紫杉二烯合成酶(GGPPS-TXS)融合蛋白,使紫杉二烯的滴度提升 54%[71]。这些结果表明,靶向区室化与蛋白融合技术可有效突破紫杉烷生产的限制瓶颈。此外,转录因子调控在紫杉烷生物合成优化中同样发挥关键作用。例如,在红豆杉叶片中过表达转录因子基因TcWRKY33,可显著提高 10 - 去乙酰巴卡亭 III 的积累量 [72];在红豆杉悬浮细胞中过表达TcMYB29a基因,不仅促进紫杉醇的积累,还能上调紫杉醇生物合成关键基因的表达水平 [73]。
紫杉烷的生物合成与化学合成耦合策略
除单一生物合成策略外,生物 - 化学合成耦合技术已成为解决 P450 酶催化宽泛性问题的有效方案 [19,74]。该策略既利用生物合成的精准性生产紫杉醇前体,又借助化学合成的稳定性,绕过那些难以在体外重构的酶促反应步骤。该杂合策略的核心技术之一是无细胞蛋白合成系统(CFPS),其利用体外反应平台与纯化酶或细胞提取物催化目标代谢反应 [75]。与体内合成系统不同,无细胞蛋白合成系统可规避中间产物引发的细胞毒性,消除内源代谢途径的竞争,并能直接优化反应条件以最大化酶活性 [76]。这些特性使该系统成为生产紫杉烷前体、突破 P450 酶相关限制的理想工具。例如,李氏团队开发了一套整合无细胞酶促反应、化学催化与全细胞催化的杂合合成系统,用于紫杉烷的合成 [74]。该系统成功绕过 T5αH 与紫杉二烯 - 5α- 醇 - O - 乙酰转移酶(TAT)的催化瓶颈,以甲羟戊酸为起始原料,合成出三种紫杉醇关键中间体:紫杉二烯、紫杉 - 4 (20),11 (12)- 二烯 - 5α- 乙酸酯(T5α-AC)与紫杉 - 4 (20),11 (12)- 二烯 - 5α,10β- 二醇 - 5 - 乙酸酯(T5α-AC-10β-ol)。值得注意的是,该整合系统不仅最大限度减少了副产物生成,获得了目前已报道的最高 T5α-AC-10β-ol 产量,还通过优化紫杉烷 - 10β- 羟化酶(T10βH)在酿酒酵母中的表达,使 T5α-AC 的滴度较传统发酵工艺提升超过 2000 倍。
人工合成微生物菌群:提升紫杉烷产量的新策略
人工合成微生物菌群是由两种或两种以上野生型或基因工程改造的微生物菌种共培养形成的群落 [77]。这类菌群可通过物种间协同作用[78],执行复杂的代谢任务,有效解决单一微生物系统在应对紫杉醇长程多步生物合成途径时的局限性。通过利用微生物间的协同效应,菌群策略能够提升反应效率,增加紫杉烷产量。例如,周氏团队将该策略应用于紫杉烷生产,构建了大肠杆菌 - 酿酒酵母双菌种共培养体系[36]。在该体系中,大肠杆菌负责合成紫杉二烯,产物可被动跨膜转运至酿酒酵母细胞内;酿酒酵母则利用其自身的 P450 酶(如 T5αH),催化前体物质氧化生成结构更复杂的紫杉烷中间体。该设计充分发挥了两种微生物的独有优势:大肠杆菌可高效合成紫杉烷前体,而酿酒酵母能提供适合 P450 酶表达的真核生物环境,从而克服 P450 酶在原核系统中难以适配的问题。该菌群策略的优势体现在三方面:第一,可对紫杉醇生物合成途径的不同模块进行独立优化,简化工程改造流程,加速紫杉烷中间体生物合成的研究进程;第二,最大程度利用不同微生物在紫杉烷生产中的专属特性;第三,通过将紫杉醇生物合成途径在不同菌种间进行空间分隔,有效减轻反馈抑制作用。
紫杉醇生物合成策略的利弊权衡
在适配性微生物系统中重构复杂的紫杉醇生物合成途径,核心在于使途径组分与微生物代谢系统相适配。目前研究通过靶向工程改造,主要解决三大核心挑战:前体供应不足、P450 酶催化氧化效率低下及代谢流竞争。每种解决方案均存在独特的利弊权衡,需经过审慎评估后再选用。例如,异戊烯醇利用途径(IUP)通过外源前体供应,避免与宿主内源代谢途径竞争,但与经工程改造的 MVA/MEP 途径相比,其工业化应用的经济性偏低;人工合成微生物菌群虽能解决 P450 酶的适配性问题,但面临菌群种群动态平衡与细胞间代谢物转运的挑战。值得注意的是,这些策略并非相互排斥,而是可通过分阶段技术路线图实现协同整合:在途径重构初期,生物 - 化学杂合策略可加速概念验证进程;而最具应用前景的方案,则是整合三项核心技术 —— 经工程化改造的 MVA 途径(保障前体稳定供应)、优化的 P450 酶系统(实现高效氧化反应),以及动态调控技术(最大化流向紫杉醇的碳代谢流)。这种整合策略既能攻克当前紫杉烷生产的瓶颈,又能为未来技术创新提供灵活的框架。
紫杉醇从头生物合成宿主的理性选择
选择合适的宿主进行紫杉烷生物合成,需使宿主固有的生物学特性与紫杉醇生物合成途径的独特需求相匹配。紫杉醇合成途径对宿主有三项关键要求:其一,该途径近半数反应由细胞色素 P450 酶催化,这类酶需要类真核生物环境以实现正确折叠,同时需要持续的 NADPH 供应以维持催化活性;其二,多步级联反应需要靶向性的亚细胞区室化,以避免过度氧化副产物生成导致的代谢流分流;其三,晚期中间体的合成需要持续的萜类前体供应,以防止下游修饰反应出现瓶颈。尽管科研人员已在大肠杆菌、酵母、本氏烟草及蓝细菌等异源宿主中取得显著进展,实现了紫杉二烯、紫杉二烯 - 5α- 醇等关键前体的从头合成(见表 1),但在异源底盘生物中完整重构紫杉醇生物合成途径的目标仍未达成。这也凸显了为紫杉醇从头合成理性选择宿主的关键意义。
经典微生物底盘:大肠杆菌与酵母
大肠杆菌是代谢工程领域应用最广泛的原核底盘生物,其优势在于生长速度快、可扩展性强、基因操作工具成熟。该宿主已被成功用于构建紫杉醇关键前体的合成菌株,产物包括紫杉二烯 [43,45]、巴卡亭 III(需以 10 - 去乙酰巴卡亭 III 为底物)[79] 及其他氧化型紫杉烷中间体 [37]。一项代表性研究通过模块化表达调控,实现了大肠杆菌内源 MEP 途径与异源紫杉二烯合成模块的计算指导型动态平衡,最终使紫杉二烯产量提升约 15000 倍。该研究将大肠杆菌内源代谢与工程化途径进行系统性整合,精准地将萜类前体库导向紫杉二烯合成,为紫杉醇的规模化生物制造奠定了基础 [5]。然而,大肠杆菌缺乏膜结合型细胞器,且翻译后修饰机制有限,而这两者正是紫杉醇晚期氧化步骤不可或缺的条件 [80]。因此,尽管大肠杆菌适用于上游前体(如 GGPP、紫杉二烯)的生产,但作为单一底盘生物,其固有局限性使其难以实现紫杉醇的从头生物合成。
与之相对,酿酒酵母作为真核底盘生物,具备内源的细胞器区室化系统、完善的翻译后修饰机制、优异的发酵耐受性,且拥有公认安全(GRAS)认证。这些特性使其能够实现植物源 P450 酶的功能性表达,成为紫杉烷生物合成领域极具应用潜力的工业底盘。基于酿酒酵母的紫杉烷研究主要围绕两个方向展开:优化前体(如紫杉二烯)产量,以及攻克氧化型紫杉烷中间体合成的途径缺口。在紫杉二烯合成方面,抑制竞争性固醇合成途径、关键酶分子改造、为酶匹配适配性启动子以优化基因表达等策略,均被证实可有效提升紫杉二烯产量 [46,48]。除前体生产外,酿酒酵母还为解析紫杉醇晚期氧化步骤提供了重要支撑。杨氏团队的研究揭示了紫杉醇合成的羟基化顺序为C5→C10→C13/C9α,并鉴定出 CYP725A55 酶 —— 该酶可通过级联氧化与协同酰基重排机制,催化氧杂环丁烷酯的形成;同时,研究人员新发现的一种 C7 位特异性乙酰转移酶,首次实现了以紫杉 - 4 (20),11 (12)- 二烯 - 5α- 醇为原料,在工程酵母中完整合成紫杉醇的含氧四环核心结构 ——1β- 去羟基巴卡亭 VI [20]。该研究填补了紫杉醇晚期氧化途径长期存在的认知空白。
除传统酿酒酵母外,解脂耶氏酵母作为一种非常规酵母,也展现出良好的应用前景。例如,徐氏团队的研究 [53] 证实,通过 “推拉” 代谢策略,解脂耶氏酵母可显著提升紫杉二烯产量。尤为关键的是,近期研究验证了解脂耶氏酵母在萜类化合物合成方面的优势,包括通过过氧化物酶体工程实现角鲨烯途径的区室化 [81],以及通过结构指导的定点突变克服番茄红素环化酶的抑制作用 [82]—— 这些技术均是合成复杂萜类骨架的关键适配手段。
非常规微生物底盘:光合藻类、枯草芽孢杆菌与链格孢菌
蓝细菌作为光合自养型生物,能够将太阳能与二氧化碳转化为高附加值生物化学品,是极具潜力的底盘生物 [83]。其代谢灵活性体现在拥有强大的内源 MEP 途径,可高效供应萜类前体 [84,85]。蓝细菌的光合电子传递链能够再生还原力(如 NADPH),提升 P450 酶的催化活性,从而促进 P450 酶在蓝细菌宿主中的整合;同时,其类囊体膜可为植物源真核 P450 酶的功能性表达提供理想环境,这使蓝细菌成为紫杉烷生物合成领域极具创新性的稳健平台 [86]。近期一项研究证实了蓝细菌底盘在紫杉烷生产中的潜力:钟氏团队在集胞藻 PCC 6803中成功整合并优化了一条异源生物合成途径,实现了紫杉二烯与 T5α- 醇的显著积累 [59]。该研究确立了蓝细菌作为紫杉醇前体可持续、稳健生产底盘的应用价值。
除蓝细菌外,枯草芽孢杆菌与链格孢菌作为替代性微生物底盘,同样具有独特优势。枯草芽孢杆菌是一种 GRAS 认证菌株,已被证实可用于天然产物的生物合成,包括紫杉二烯的生产 [58]。尽管其合成生物学工具的开发程度落后于大肠杆菌(尤其是缺乏稳定的基因表达系统),但凭借其广泛的代谢能力与近年来的基因技术突破,枯草芽孢杆菌仍是紫杉烷途径工程改造的可行候选底盘。与此同时,丝状真菌链格孢菌拥有成熟的转化体系,是另一类极具潜力的紫杉烷生物合成平台 [57]。
植物细胞底盘
与微生物系统不同,植物细胞天然具备支撑多步植物源 P450 酶参与的复杂代谢途径的能力。例如,科研人员利用本氏烟草 [18]、拟南芥 [56]、番茄 [87] 及青蒿 [88] 等植物底盘的成熟遗传转化体系,成功构建了紫杉二烯与紫杉二烯 - 5α- 醇的生物合成途径。其中,本氏烟草因生长速度快、生物量大且支持瞬时基因表达,已成为模式植物研究的核心系统 [14],是植物天然产物合成酶功能鉴定与合成途径重构的理想宿主 [55]。通过将紫杉醇生物合成基因导入本氏烟草,研究人员已阐明多个紫杉醇合成相关酶的功能 [18]。一项标志性研究中,蒋氏团队在本氏烟草中实现了紫杉醇前体巴卡亭 III的生产 [12]。研究人员通过瞬时表达紫杉烷氧杂环丁烷合成酶(TOT)、紫杉烷 - 9α- 羟化酶(T9αH),以及另外 7 个已知功能基因(TXS、T5αH、T13αH、T2αH、T7βH、TAT与TBT),证实了植物底盘具备重构复杂生物合成途径的能力。此外,安特罗拉(Anterola)团队将短叶红豆杉来源的 TXS 基因在小立碗藓中表达,成功合成紫杉醇前体紫杉 - 4 (5),11 (12)- 二烯,并提出小立碗藓可作为紫杉醇及其前体生物制造的潜在宿主 [89]。
除完整植株系统外,植物悬浮细胞也是生产高附加值植物源代谢物的优良宿主 [90]。在紫杉烷生产领域,红豆杉属植物细胞培养技术已取得显著进展。红豆杉悬浮细胞是紫杉醇及其前体的天然来源,其规模化培养技术的突破推动了紫杉醇的工业化生产。马塔斯(Matas)团队利用发根农杆菌 A4 菌株,成功建立了欧洲红豆杉的稳定离体转基因株系 [91]。通过过表达BAPT、DBTNBT等紫杉醇合成晚期基因,研究人员使紫杉醇滴度提升 4 倍。此外,法顿生物科技等企业已成功利用该技术,通过优化细胞培养工艺实现紫杉醇的工业化生产。除基因过表达策略外,转运蛋白工程是提升红豆杉悬浮细胞紫杉醇产量的另一关键技术 [92]。紫杉醇毒性中间体的胞内积累往往会限制紫杉烷的生产效率,而功能性转运蛋白可促进这些中间体或紫杉醇的胞外分泌,从而降低细胞毒性,优化流向紫杉醇的代谢流。近期一项针对南方红豆杉的研究,通过单细胞 RNA 测序与基质辅助激光解吸电离成像质谱(MALDI-IMS)分析,鉴定出一个潜在的紫杉醇转运蛋白基因 ——ABCG2[93]。该基因在表皮细胞、内皮细胞与木质部薄壁细胞中特异性表达,且与紫杉醇生物合成基因的表达区域共定位,推测其可能参与紫杉醇的靶向转运,有望成为后续工程改造的分子靶点。
紫杉烷生产底盘的综合对比与利弊权衡
选择合适的宿主系统合成紫杉醇等高附加值复杂天然产物,需要采用战略性的多维度评估方法(见表 1)。总体而言,不同底盘生物均具备适配紫杉醇生物合成不同阶段的独特优势,同时也存在制约其单独应用的固有局限性。例如,大肠杆菌可通过 MEP 途径工程改造实现紫杉二烯的克级产量(最高达 1.2 g/L),但缺乏 P450 酶折叠所需的内质网结构;酿酒酵母借助内质网区室化支持 P450 酶活性,却面临与内源固醇合成途径的代谢流竞争;蓝细菌以二氧化碳为可持续碳源合成前体,但生长速度较慢;红豆杉悬浮细胞保留了完整的内源紫杉醇合成途径,却存在工业化生产成本高昂的问题。上述利弊权衡关系决定了紫杉烷生产需要针对性的工程改造策略,而非 “一刀切” 的通用底盘。为解决这一矛盾,人工合成微生物菌群成为新兴技术范式 —— 该策略将紫杉醇合成途径的不同模块分配给天然适配特定任务的宿主。例如,前文所述的大肠杆菌 - 酿酒酵母双菌种共培养体系,即可实现高效紫杉烷生产 [36]:大肠杆菌凭借高效的萜类代谢途径,负责合成紫杉烷初始前体(如紫杉二烯);酵母则擅长表达植物源 P450 酶,主导紫杉醇合成的晚期氧化步骤。这种 “分工协作” 模式既减轻了单一宿主的代谢负担,又充分发挥了各底盘的独有优势,包括原核生物的代谢流优势、真核生物的 P450 酶功能优势,以及与植物途径的适配优势。
人工智能指导的代谢途径与底盘细胞优化
将机器学习(ML)技术整合到靶向代谢途径优化中,具有巨大潜力,但该技术在紫杉醇生物合成途径构建中的应用仍有待深入探索。通过将机器学习与酵母特异性基因组装策略相结合,研究人员可快速攻克酵母中紫杉醇生物合成的核心瓶颈,如异源基因表达失衡与代谢流分流等问题(见图 4)。值得关注的是,MiYa 平台(整合机器学习与酵母基因元件组装技术)的应用案例表明,通过优化酵母中的组合基因表达水平,可显著提升目标紫杉烷产量 [94]。与之类似,基于机器学习的策略已被用于优化异源基因拷贝数,使解脂耶氏酵母的二十碳五烯酸产量达到 27.5 g/L [95]。这些技术进展表明,机器学习策略同样可用于优化酵母及其他微生物底盘中的紫杉醇生物合成途径构建。机器学习技术还有望解决紫杉醇生物合成的关键瓶颈 —— 即介导紫杉醇关键氧化步骤的 P450 酶(如 T5αH)的高催化宽泛性与低活性问题。例如,贝叶斯优化引导的进化算法(BO-EVO)可通过迭代探索蛋白质的适配性景观,实现 P450 酶功能的精准优化 [96];而EVOLVEpro 方法整合了蛋白质语言模型与小样本学习框架,即使在实验数据有限的情况下,也能高效提升 P450 酶的功能 [97]。尽管这些工具尚未直接应用于紫杉醇特异性 P450 酶的优化,但其在其他天然产物合成途径 P450 酶活性优化中的成功案例 [98,99],预示着它们在紫杉醇生物合成研究中具有广阔的应用前景。
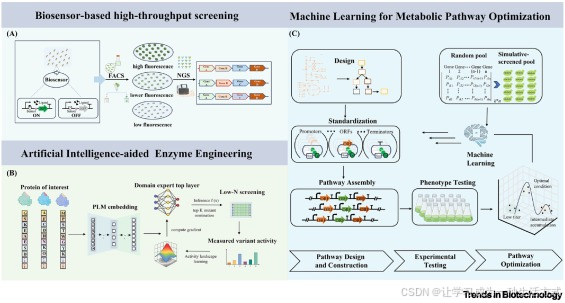
图 4 人工智能驱动的紫杉烷生物合成增效策略示意图
(A)生物传感器介导的高通量筛选:目标紫杉烷中间体与基因编码型生物传感器结合后,可触发荧光信号的产生。研究人员首先构建紫杉烷生物合成基因的随机突变文库,随后利用荧光激活细胞分选技术(FACS),根据荧光信号强度(高、中、低)对突变文库进行分选。最后通过新一代测序技术(NGS),筛选鉴定出紫杉烷生物合成相关的关键基因(如基因 a、基因 b、基因 c)。
(B)EvolvePro 酶分子进化平台示意图:该迭代优化流程始于目标酶的低通量诱变;预训练的蛋白质语言模型(PLM)通过氨基酸残基水平的特征提取,生成酶蛋白的结构嵌入特征向量;对功能区域内的特征向量进行位置平均后,获得酶蛋白的结构域特异性表征;再利用实验验证的酶活性数据训练回归模型(K代表批次大小;f(x)代表预测得分)。在主动学习循环中,每一轮筛选获得的最优突变体(选取排名前n的突变体),可反向用于更新蛋白质语言模型的参数,由此构建闭环优化系统(如虚线箭头所示)。
(C)机器学习辅助的代谢途径优化:途径优化分为三个连续阶段:(i)设计阶段:利用 Golden Gate 组装技术,将启动子 - 开放阅读框 - 终止子(PRO-ORF-TER, POT)元件模块化;(ii)测试阶段:在可控发酵条件下,对表型鉴定后的菌株文库进行产物滴度定量检测;(iii)优化阶段:构建梯度提升回归模型,建立元件组合方式与产物滴度的关联图谱,并基于模型的预测置信区间,指导组合参数的优化调整。这种计算模拟与实验验证的整合策略,可实现生物合成效率的系统性提升。
缩写注释
AI:人工智能;FACS:荧光激活细胞分选技术;ML:机器学习;NGS:新一代测序技术;ORF:开放阅读框;PLM:蛋白质语言模型;PRO:启动子;TER:终止子。
在紫杉烷生产酵母底盘的优化过程中,机器学习技术同样为突破酵母底盘的固有局限提供了有效方案。尽管酵母被广泛应用于微生物源紫杉烷的合成,但在紫杉醇生物合成中仍面临特有挑战,例如紫杉烷中间体的毒性积累、紫杉醇合成所需萜类前体供应不足等问题。
以卷积神经网络(CNN)和长短期记忆网络(LSTM)为代表的深度学习模型,已被证实可有效改善酵母中与萜类合成相关的细胞功能。例如,通过预测最优基因组合,研究人员实现了酵母过氧化物酶体功能的改良:将甲羟戊酸途径的酶类靶向定位到过氧化物酶体后,异戊二烯衍生物香叶醇的产量提升 80%[61]。
然而,机器学习在紫杉醇生物合成领域的应用仍面临一大核心挑战 —— 高质量标准化数据集的匮乏,而这类数据集是训练模型以精准预测和优化紫杉醇生物合成途径的关键。为解决这一问题,本研究建议构建紫杉醇生物合成领域的协作式开放数据资源库,供全球科研人员共享、获取和整合紫杉醇生物合成相关的全面数据集,从而推动该领域的开放式协同研究。
结论与未来展望
紫杉醇及其衍生物(如多西他赛、卡巴他赛)仍是临床上不可或缺的抗癌药物,但其从头生物合成的可持续生产,仍受限于尚未解决的认知空白与技术壁垒(详见亟待解决的关键问题)。目前,三项相互关联的核心挑战仍未攻克:
第一,紫杉醇生物合成途径复杂且部分环节尚未阐明,严重阻碍了理性代谢工程改造的推进。紫杉醇的生物合成大概率是一个高度分支的代谢网络,其中羟基化、氧化、酰基化等酶促反应的先后顺序仍有待明确;
第二,植物源合成途径与微生物底盘的适配性差,限制了异源紫杉烷的生产效率。植物源 P450 酶在微生物系统中往往催化活性不足,同时生成大量分流代谢流的副产物,干扰异源紫杉醇合成途径的重构;
第三,紫杉烷中间体的固有细胞毒性超出宿主耐受范围,限制了产物的胞内积累,由此形成一个固有矛盾:紫杉醇的抗癌活性同时也会抑制其生产宿主的生长。
为攻克上述挑战,未来研究应聚焦于三大核心目标:(i)优化异源酶(尤其是 P450 酶)的功能性表达;(ii)提高关键紫杉烷前体的胞内可利用度;(iii)突破紫杉醇生物合成中现存的代谢瓶颈。
从前瞻性视角来看,两项策略将对紫杉醇生物合成的发展起到关键推动作用:人工合成微生物菌群技术与人工智能指导的酶分子工程技术。人工合成微生物菌群(如大肠杆菌 - 酿酒酵母共培养体系)可通过代谢分工协作,突破单一底盘的局限性,是实现紫杉烷规模化生产的最具可行性的中期技术平台。与此同时,基于人工智能的工具(如 EvolvePro 平台)可用于优化限速酶(如 T5αH),降低 P450 酶的产物宽泛性,从而直接提升流向目标前体的代谢流,为紫杉醇的从头合成奠定基础。
除上述核心策略外,转运蛋白工程与被动分泌机制的研究,也值得在紫杉醇外排领域进一步探索。具体而言,尽管有研究推测南方红豆杉来源的 ABCG2 转运蛋白介导紫杉醇的外排,但目前支持该功能的证据仍较为匮乏,其体外转运活性也尚未得到验证。另一方面,紫杉醇的脂溶性特性使其具备被动分泌的潜力 —— 双相反应器(如添加植物油上层覆盖相的反应器)高效回收紫杉烷的实验结果,也印证了这一点。因此,未来研究应优先明确紫杉醇外排的主导途径。
底盘优化同样至关重要:基于 CRISPR 的基因组编辑技术,可用于调控辅酶 / 辅因子的供应,进而提升前体库容量与酶活性。对于难以突破的代谢瓶颈,化学酶法协同策略可作为连接生物合成灵活性与化学合成稳定性的桥梁。最后,深入解析紫杉醇生物合成的转录与转录后调控机制,是实现紫杉醇稳定、高产、工业化生产的必要前提。
亟待解决的关键问题
大肠杆菌、酵母、蓝细菌、植物细胞等不同底盘生物在紫杉醇生物合成中各有哪些优势与局限性?综合考量合成效率、可扩展性及代谢适配性等因素,哪种底盘生物最具潜力成为紫杉醇从头合成的平台?
如何利用先进人工智能系统整合紫杉醇生物合成的多组学数据,预测未知的途径分支以解决途径模糊性问题?如何将人工智能获得的研究洞见进一步应用于合成生物学工具的改良,以及指导紫杉醇从头合成底盘的理性设计?
采用何种策略,能够在微生物及植物底盘系统中提高细胞色素 P450 酶(如 T5αH)等关键合成酶的异源催化效率,并降低其产物宽泛性?
鉴于紫杉醇生物合成代谢网络的高度分支化与复杂性,应通过哪些策略系统性鉴定并优化关键节点与途径,以提升紫杉醇前体的整体合成效率?
如何整合无细胞蛋白合成系统、人工代谢合成模块及化学酶法合成技术,突破紫杉醇生物合成的现存瓶颈,实现紫杉醇前体可持续、规模化且经济可行的生产?
更多推荐
 已为社区贡献24条内容
已为社区贡献24条内容








所有评论(0)