AI+Medicine文章分享:DeepRare:罕见病诊断智能系统
本文提出首个基于大语言模型的罕见病诊断系统DeepRare,采用三层架构整合临床描述、HPO术语和基因检测等多源数据,通过自反思诊断循环生成可追溯的疾病诊断排名。在涵盖2919种疾病的6401个病例测试中,对1013种疾病实现100%诊断准确率,HPO单模态任务Recall@1达57.18%,多模态任务达70.60%,显著优于现有方法。临床专家验证其推理链一致性达95.40%,系统已部署为网页应用
文章来源:https://arxiv.org/abs/2506.20430
一段话总结
本文提出首个基于大语言模型(LLM)的罕见病诊断智能系统DeepRare,该系统可处理自由文本临床描述、结构化HPO术语、VCF格式基因检测结果三类异质输入,通过“中央主机+专业代理服务器+多源外部数据”的三层架构,生成带可追溯推理链的疾病诊断排名;在涵盖8个数据集、2919种疾病、6401个病例(含亚洲、北美、欧洲多中心数据)上评估,对1013种疾病实现100%诊断准确率,HPO单模态任务Recall@1达57.18%(超次优方法23.79个百分点),HPO+基因多模态任务Recall@1达70.60%(超Exomiser的53.20%),且临床专家对其推理链的验证一致性达95.40%,目前已部署为网页应用(http://raredx.cn/doctor),为罕见病临床诊断提供可解释、高可信的AI辅助工具。
思维导图
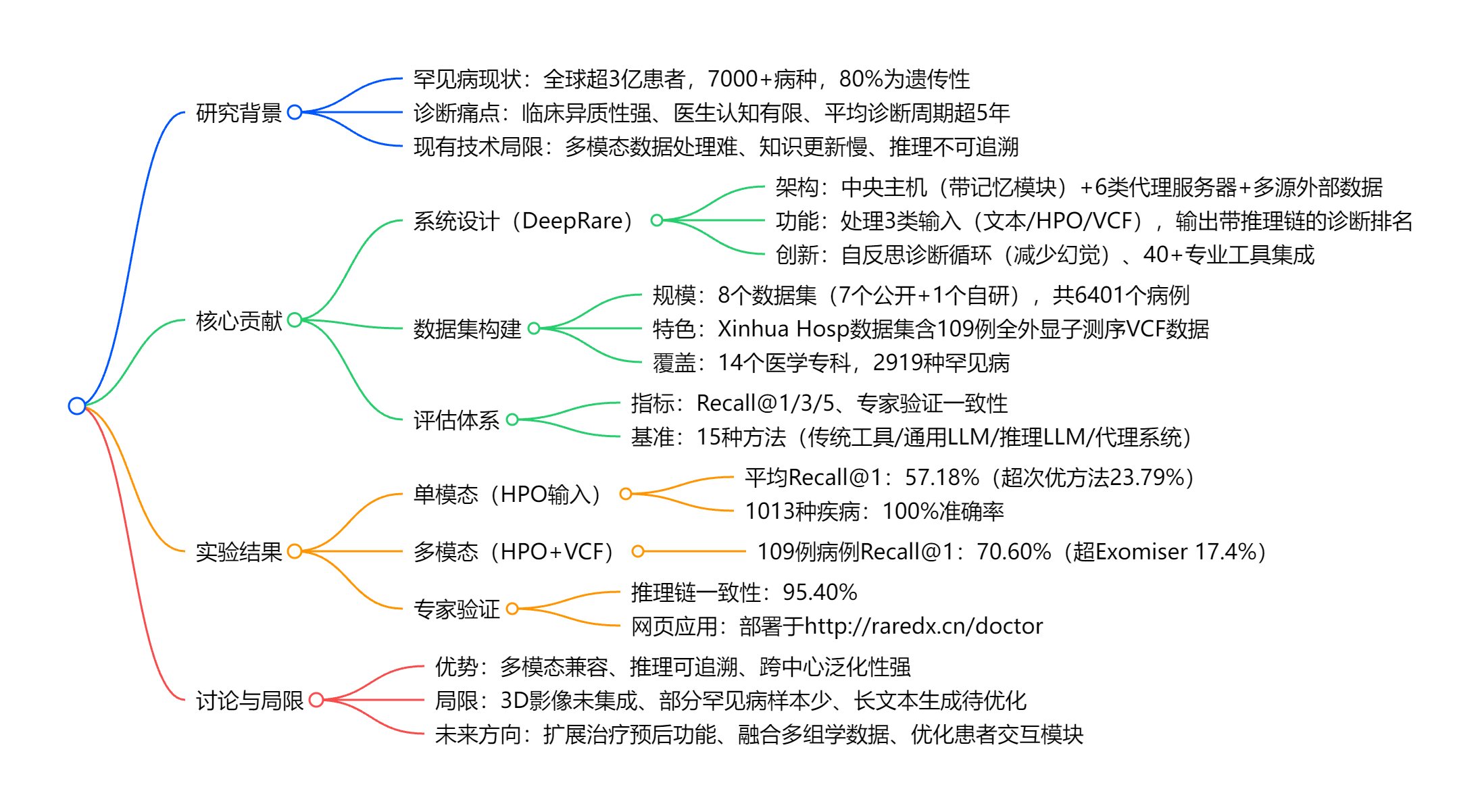 详细总结
详细总结
研究背景与挑战
罕见病虽单病种发病率低(<1/2000人),但全球累计影响超3亿人,已发现超7000种病种,其中80%为遗传性疾病。当前诊断面临四大核心挑战:
- 临床复杂性:症状异质性强,常涉及多系统病变,需跨学科知识整合;
- 数据稀缺性:单病种样本量少,模型易过拟合,难以覆盖罕见亚型;
- 知识动态性:国际罕见病研究联盟(IRDiRC)数据显示,每年新增260-280种罕见遗传病,传统模型难以及时更新;
- 推理透明度:临床诊断需可追溯的证据链,但现有工具多仅输出疾病列表,缺乏中间推理过程,医生难以信任。
核心贡献一:DeepRare系统架构设计
DeepRare采用三层模块化架构,实现“数据输入-分析推理-结果输出”的全流程自动化,具体组件如下表:
| 架构层级 | 核心组件 | 功能描述 | 关键技术 / 工具 |
|---|---|---|---|
| 中央主机 | LLM 驱动的协调单元 + 长时记忆模块 | 1. 调度代理服务器执行任务 2. 存储中间结果与证据 3. 执行自反思诊断循环 |
基础模型:DeepSeek-V3/GPT-4o 等 记忆更新:增量式证据存储 |
| 代理服务器 | 6 类专业代理(共集成 40 + 工具) | - 表型提取器:文本→标准化 HPO 术语 - 疾病标准化器:映射至 Orphanet/OMIM - 知识检索器:实时获取文献 / 指南 - 病例检索器:匹配相似临床案例 - 表型分析器:调用专业诊断工具 - 基因型分析器:VCF 注释与变异排序 |
BioLORD(HPO 映射)、Exomiser(VCF 分析)、PubMedRetriever(文献检索) |
| 外部数据源 | 医学文献 / 知识库 / 病例库 / 基因数据库 | 提供可验证的诊断证据,确保推理追溯性 | 文献:PubMed/Google Scholar 知识库:Orphanet/OMIM/HPO 病例库:MIMIC-IV-Rare/Xinhua Hosp 基因库:gnomAD/ClinVar |
关键创新:自反思诊断循环
系统通过 “信息收集→初步诊断→证据验证→循环优化” 四步流程,减少 LLM 幻觉与误诊风险:
- 信息收集:代理服务器获取表型 / 基因型相关证据(如 HPO 匹配文献、VCF 变异注释);
- 初步诊断:中央主机基于证据生成候选疾病列表;
- 证据验证:知识检索器针对候选疾病补充最新文献,验证诊断合理性;
- 循环优化:若候选疾病均不满足证据要求,增大检索深度(N+ΔN),重新收集信息,直至生成有效诊断。
核心贡献二:多源数据集构建
研究整合 8 个数据集(7 个公开 + 1 个自研),覆盖全球多中心病例,具体信息如下表:
| 数据集名称 | 病例数 | 疾病数 | 输入类型 | 来源地区 | 公开性 | 核心特点 |
|---|---|---|---|---|---|---|
| RareBench-MME | 40 | 17 | HPO | 文献 | 是 | 文献提取,病例典型性高 |
| RareBench-HMS | 88 | 39 | HPO | 德国( Hannover Medical School) | 是 | 临床中心数据,症状复杂度高 |
| RareBench-LIRICAL | 370 | 252 | HPO | 文献 | 是 | 含详细表型 - 基因关联 |
| RareBench-RAMEDIS | 624 | 74 | HPO | 科学家上传 | 是 | 罕见代谢病专项 |
| MyGene2 | 146 | 58 | HPO + 基因 | 患者上传 | 是 | 含候选致病基因信息 |
| DDD | 2283 | 2150 | HPO | 文献 | 是 | 最大公开罕见病数据集 |
| MIMIC-IV-Rare | 1875 | 355 | HPO | 美国(Beth Israel Deaconess Medical Center) | 是 | 住院病历提取,含随访信息 |
| Xinhua Hosp(自研) | 975 | 314 | HPO+VCF(109 例) | 中国(上海新华医院) | 否 | 含全外显子测序数据,唯一带 VCF 的测试集 |
核心贡献三:全面评估体系与实验结果
评估基准与指标
- 对比方法:15 种主流方法,分为四类:
- 传统工具:PhenoBrain(HPO 分析)、PubCaseFinder(病例匹配);
- 通用 LLM:GPT-4o、DeepSeek-V3、Gemini-2.0-flash;
- 推理 LLM:Claude-3.7-Sonnet-thinking、DeepSeek-R1;
- 代理系统:MDAgents(多学科协作)、DeepSeek-V3-Search(带搜索功能)。
- 核心指标:
- 诊断准确率:Recall@1(Top-1 命中)、Recall@3、Recall@5;
- 推理可信度:临床专家对推理链的验证一致性(10 位副主任医师,5 年以上经验)。
关键实验结果
-
HPO 单模态诊断(无基因数据)
- 平均性能:Recall@1 57.18%、Recall@3 65.25%,超次优方法(Claude-3.7-Sonnet-thinking)23.79、18.65 个百分点;
- 数据集表现:在 RareBench-MME(40 例)中 Recall@1 达 70.0%,在 Xinhua Hosp(975 例)中达 58.0%,泛化性显著;
- 疾病覆盖:对 2919 种疾病中的1013 种实现 100% 诊断准确率,主要为症状典型的单基因病(如维生素 B12 反应性甲基丙二酸血症)。
-
HPO+VCF 多模态诊断(109 例全外显子测序病例)
结果显示:DeepRare 多模态性能显著优于传统工具与通用 LLM,因整合了基因变异的致病性分析(如 ACMG 分级)与表型关联证据。方法 Recall@1 Recall@3 Recall@5 DeepRare 70.60% 81.70% 88.10% Exomiser(传统工具) 53.20% 67.90% 75.20% GPT-4o(通用 LLM) 42.20% 58.70% 65.10% -
专家验证结果
- 推理链一致性:180 个随机病例中,专家与 DeepRare 的证据引用一致性达95.40%;
- 错误分析:仅 4.6% 不一致源于两类问题 ——①系统生成不存在的文献 URL(幻觉);②诊断结论错误导致引用无关文献。
临床应用:网页应用部署
为降低临床使用门槛,DeepRare 已部署为用户友好的网页应用(http://raredx.cn/doctor),流程分为五步:
- 临床数据录入:输入患者年龄、性别、家族史、症状描述,支持上传病例报告、影像、VCF 文件;
- 系统症状问询:AI 引导补充器官受累范围、症状进展时间等细节,缩小诊断范围;
- HPO 术语映射:自动将文本症状转为标准化 HPO 术语,支持医生手动调整;
- 诊断分析输出:生成带证据链的 Top-5 疾病排名,每条诊断含 3-4 条参考文献(如 Orphanet 条目、PubMed 文献);
- 报告下载:导出 PDF/Word 格式诊断报告,可直接整合入电子病历系统。
局限性与未来方向
现存局限
- 数据层面:3D 影像(如 CT/MRI)未集成,且部分超罕见病(发病率 < 1/10 万)样本仍不足;
- 功能层面:仅支持诊断,未涵盖治疗方案推荐、预后预测等临床全流程需求;
- 生成层面:长文本(如完整诊断报告)生成质量待提升,部分输出缺乏病变位置等细节(如 “左侧肺部结节” vs “肺部结节”)。
未来计划
- 数据扩展:通过 GAN / 扩散模型合成超罕见病数据,补充 3D 影像与多组学(转录组、代谢组)数据;
- 功能升级:扩展治疗推荐模块,整合 ClinicalTrials.gov 的罕见病试验信息;
- 模型优化:增大 LLM 参数规模(如从 14B 升级至 70B),优化自反思循环的证据筛选逻辑。
更多推荐
 已为社区贡献1条内容
已为社区贡献1条内容







所有评论(0)