卡梅德生物技术快报|哺乳动物细胞蛋白表达:载体构建、筛选与细胞工程实战指南
本文聚焦哺乳动物细胞蛋白表达核心技术体系,系统讲解宿主选择、载体设计、高通量筛选、细胞工程改造等关键环节,为生物制药研发人员提供可落地的技术方案,助力高效稳定细胞株构建。哺乳动物细胞蛋白表达是载体、筛选、细胞工程、培养工艺协同的系统工程。当前表达量已达克级水平,未来结合基因编辑、系统生物学、AI 培养调控,将进一步提升效率、降低成本,为生物制药提供更强技术支撑。参考文献:王登,刘煜。用于重组蛋白表
摘要
本文聚焦哺乳动物细胞蛋白表达核心技术体系,系统讲解宿主选择、载体设计、高通量筛选、细胞工程改造等关键环节,为生物制药研发人员提供可落地的技术方案,助力高效稳定细胞株构建。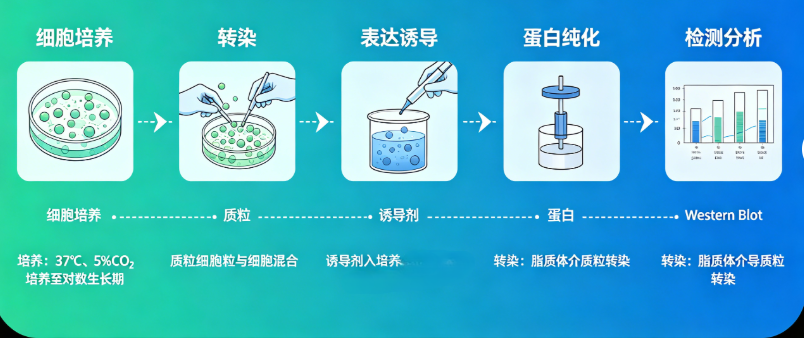
1 哺乳动物细胞蛋白表达:宿主选型与技术定位
哺乳动物细胞蛋白表达是重组治疗性蛋白研发与生产的主流技术,核心优势为可完成完整翻译后修饰,保证蛋白结构、活性与安全性接近人源天然蛋白。在工业与实验室场景中,常用宿主细胞及定位如下:
- CHO 细胞:工业化首选,支持无血清悬浮培养、基因扩增,糖基化匹配度高,市场占比超 70%;
- HEK293 细胞:实验室瞬时表达首选,转染效率高、表达速度快;
- NS0/Sp2/0 细胞:鼠源抗体表达专用宿主;
- BHK-21 细胞:适用于部分重组蛋白生产;
- PER.C6 细胞:高密度培养潜力株,灌注培养表达量可达 25 g/L。
CHO 细胞主流表达系统为 DHFR/MTX 与 GS/MSX 筛选扩增体系,通过药物加压实现基因拷贝数放大,快速获得稳定高表达株,是哺乳动物细胞蛋白表达工业化标准方案。
2 载体构建:哺乳动物细胞蛋白表达的核心设计
载体是决定哺乳动物细胞蛋白表达效率与稳定性的关键,核心目标为克服位置效应、提升转录强度、保证遗传稳定。
- 位点特异性整合技术传统随机整合易引发基因沉默,位点特异性整合(SSP)可实现精准插入,常用系统:
- Cre/loxP:支持定点整合与累积插入,适配 CHO 工程化改造;
- Flp/FRT:有效降低位置效应,提升抗体表达水平;
- RMCE:重组酶介导盒式交换,实现精准基因替换。
- 顺式作用元件优化
- IRES:实现多顺反子表达,平衡抗体轻重链比例;
- S/MARs:结合核基质,抑制基因沉默;
- UCOEs:维持染色质开放,保障长期稳定表达;
- 强启动子 / 增强子:提升转录起始效率。
采用定点整合 + 顺式元件组合设计,可显著提升表达水平与克隆均一性。
3 高通量筛选:高效获取高表达单克隆
筛选效率直接影响研发周期,工业级哺乳动物细胞蛋白表达已全面采用高通量方案:
- 有限稀释法:成本低、操作简单,但效率低;
- FACS 荧光分选:基于分泌信号快速分选,通量高;
- ClonePix FL:半固体培养基自动挑克隆,适合大规模筛选;
- 微流控芯片:单细胞可视化分离,单克隆源性可靠。
高通量筛选可将细胞株构建周期由 3 个月缩短至 1 个月内,提升研发效率。
4 细胞工程:提升哺乳动物细胞蛋白表达的关键手段
细胞工程以提升整合活细胞密度(IVCD)和细胞比生产速率(QP)为目标,分为四大方向:
- 细胞周期工程调控 p21Cip1、p27Kip1、CDC25A 等因子,使细胞停滞在 G1/S 或 G2/M 期,降低增殖、提升蛋白合成,突变 CDC25A 可使表达提升 2–6 倍。
- 代谢工程采用葡萄糖 + 半乳糖混合碳源、敲除 LDH/PDHKs、过表达谷氨酰胺合成酶等策略,减少乳酸与氨积累,优化培养环境。
- 抗凋亡工程过表达 Bcl-2 家族、IAPs 等,或敲除 Bax/Bak,提升细胞抗逆性,可使表达量提升 3–5 倍。
- 促分泌工程过表达 XBP-1、ATF4、GRP78、PDI 等,强化内质网折叠与分泌,过表达 ATF4 可使 IgG 表达提升 2.4 倍。
5 技术总结
哺乳动物细胞蛋白表达是载体、筛选、细胞工程、培养工艺协同的系统工程。当前表达量已达克级水平,未来结合基因编辑、系统生物学、AI 培养调控,将进一步提升效率、降低成本,为生物制药提供更强技术支撑。
参考文献:王登,刘煜。用于重组蛋白表达的哺乳动物细胞系的研究进展 [J]. 药物生物技术,2014, 21 (5): 478-482.
更多推荐
 已为社区贡献1条内容
已为社区贡献1条内容







所有评论(0)