Cell项目文章 | DAP-seq助力福建农林大学吴建国教授团队发现独脚金内酯信号重塑抗病毒免疫的机制
福建农林大学吴建国团队联合国际学者在《Cell》发表重要研究,揭示了独脚金内酯(SL)激素信号通路调控水稻抗病毒RNAi的新机制。研究发现SL通过激活转录因子MID1与ONAC131协同作用,上调RDR1/RDR6表达促进抗病毒小RNA产生。病毒P3蛋白通过占据SL受体D14结合界面抑制该通路,而基于冷冻电镜结构设计的D14D102N突变体可阻断P3干扰,使水稻在保持正常生长的同时获得抗病毒能力。
近日,福建农林大学吴建国教授团队联合加州大学河滨分校杰出教授丁守伟博士和清华大学闫利明研究员在Cell发表了题为 “Editing Strigolactone Hormone Receptor for Robust Antiviral Silencing in Rice”的研究论文,研究发现独脚金内酯 (SL) 激素信号传导通过转录激活RNA依赖性RNA聚合酶1 (RDR1)和RDR6,从而促进水稻植株的抗病毒沉默。爱基百客为该研究提供DAP-seq的技术支持。

研究背景
抗病毒RNAi是植物的核心防御机制,但其上游调控通路,特别是植物激素如何协调抗病毒防御,尚不完全清楚。独脚金内酯(SL)已知调控植物发育,但其在抗病毒免疫中的作用未明。
研究结果
一. SL信号传导通过维持病毒诱导的RDR1和RDR6转录激活来上调抗病毒RNAi
为了探究独脚金内酯在病毒-宿主互作中的潜在角色,研究团队结合正反向遗传学与多组学测序技术,发现一条由SL信号主导的广谱抗病毒调控链路。研究首先观察到RGSV(水稻草矮病毒)侵染会显著降低水稻内源SL含量。通过引入一系列SL信号缺陷突变体(d10, d14, d53-1D),研究证实这类材料对多种RNA病毒表现出极度易感性。反之,通过外源施加SL类似物(rac-GR24)或敲除信号抑制因子D53来激活SL信号,均能显著增强对RGSV的抗性。
小RNA测序(sRNA-seq)结果显示,RGSV感染的植物显著促进了21-nt和22-nt病毒特异性小RNA(vsiRNAs)的积累;rac-GR24处理显著增强了21-nt和22-nt vsiRNA的产生,但在所有三种SL信号缺陷水稻突变体中均受到抑制。进一步的转录组分析精准锁定了下游效应基因:病毒侵染会在SL信号依赖的前提下,特异性且大幅度地上调多个RNAi关键组分(包括RDR1和RDR6)的表达。
为了研究RDR1和RDR6在SL信号上调的抗病毒防御中的功能,研究构建了复杂的遗传材料。结果表明,如果在SL信号感知缺陷的突变体(d14)中通过组成型表达RDR1或RDR6,显著降低了RGSV的积累和疾病严重程度,并伴随vsiRNA水平的升高。这些结果表明,恢复RDR1或RDR6的表达足以挽救SL不敏感植株中的抗病毒RNAi缺陷,这支持了SL信号通过转录激活RDR1和RDR6在维持vsiRNA扩增中发挥核心作用的观点。
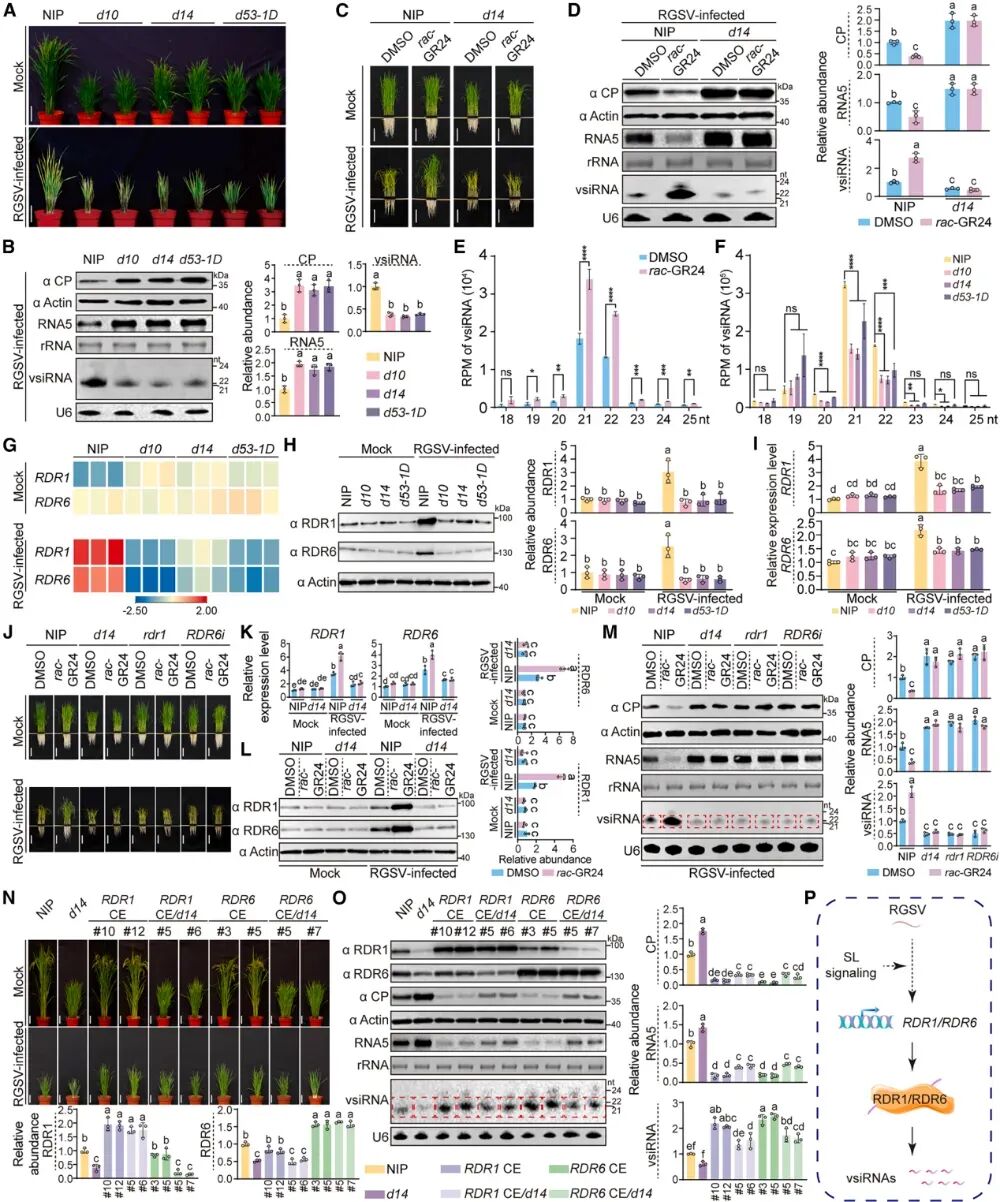
图:SL信号通过促进病毒诱导的RDR1和RDR6激活来增强抗病毒RNA干扰
二. 病毒诱导的转录因子MID1指导SL信号依赖的RDR1/RDR6转录激活及抗病毒RNA干扰
研究团队首先利用RNA-seq结合生信预测,筛选出一批受病毒诱导且具备潜在结合能力的转录因子。随后,双荧光素酶实验初步锁定了R2R3型MYB转录因子MID1。DNA亲和纯化测序(DAP-seq)结合ChIP-qPCR、MST和EMSA,在体内外多维度证实MID1能够特异地识别并结合在RDR1和RDR6启动子的保守MYB结合位点(GATAA)上,从而激活其转录。
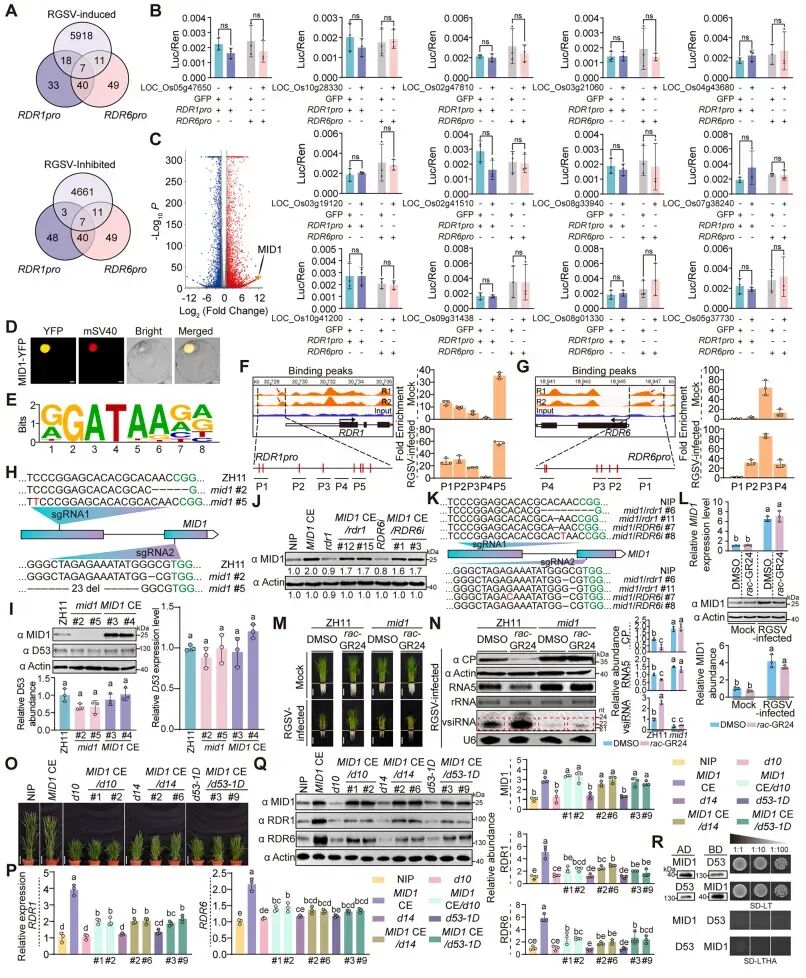
图:筛选 RGSV 诱导的RDR1和RDR6转录因子及相关转基因水稻表型
为了探究MID1的功能,研究团队构建了敲除(mid1)和过表达(MID1 CE)突变体。敲除MID1导致靶基因表达骤降、病毒大量积累;而组成型过表达MID1则出对RGSV的抗性增强。为进一步探究MID1与RDR1/6之间的遗传关系,研究构建了MID1过表达与靶基因敲除/干涉的双突变体(如MID1 CE/rdr1)。结果发现MID1 CE/rdr1和MID1 CE/RDR6i植株与rdr1和RDR6i植株一样易感,表明MID1赋予的增强抗性依赖于RDR1和RDR6。同样,mid1/rdr1和mid1/RDR6i植株在病毒易感性方面与它们的亲本植株相似,没有表现出叠加效应。这些结果提供了强有力的遗传学证据,证明MID1与RDR1和RDR6在同一途径中发挥作用,以介导抗病毒防御。
研究发现,外源施加SL类似物(rac-GR24)或SL信号突变,完全不会改变MID1自身的转录和蛋白表达水平。但是,如果缺乏SL信号(如在d14突变体中),即便人为强制过表达MID1,它也无法激活下游的RDR1/6,彻底丧失了抗病毒能力。这些发现表明,SL信号传导对于MID1介导的抗病毒防御以及RDR1和RDR6的转录激活是必不可少的,但对于由RGSV感染诱导的其自身表达则不是必需的。
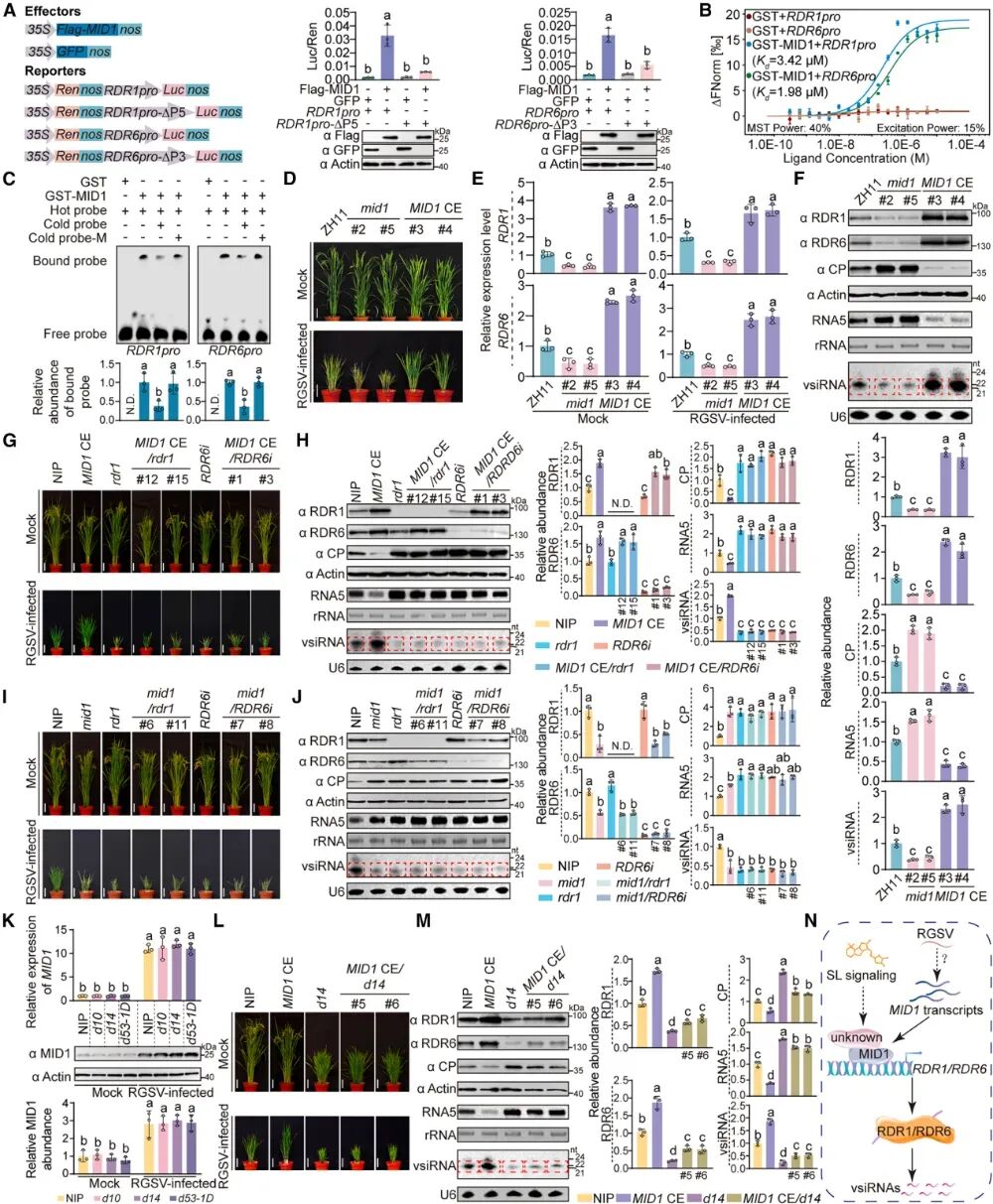
图2:MID1通过依赖SL信号通路的RDR1/RDR6激活增强水稻抗病毒RNAi
三. MID1与SL调控的NAC转录因子ONAC131协同作用以上调抗病毒RNAi
MID1的表达未影响SL通路抑制因子D53的转录或蛋白水平,且未检测到MID1与SL通路抑制因子D53蛋白之间存在物理相互作用,这表明SL信号传导通过RDR1和RDR6的转录激活过程中涉及其他调控因子。面对这种调控断层,研究将“SL缺陷突变体”与“外源SL处理(rac-GR24)”的RNA-seq数据进行了联合差异分析,筛选出12个受SL严格调控的候选因子,并最终锁定了NAC家族转录因子——ONAC131。通过Y2H、BiFC和GST Pull-down实验,确认了MID1与ONAC131在体内外存在直接的物理互作。更有意思的是,原生质体双荧光素酶实验表明:ONAC131单独无法激活RDR1/6的启动子;但如果没有ONAC131的协助,MID1的转录激活能力也会大打折扣。这表明ONAC131在MID1介导的RDR1和RDR6转录激活中发挥作用。
在敲除ONAC131的背景下强行过表达MID1(MID1 CE/onac131),植物依然表现出严重的感病表型,RDR1/6表达和vsiRNA水平均降低,说明MID1赋予的抗性完全依赖于ONAC131的存在。反之,在敲除MID1的背景下过表达ONAC131(ONAC131 CE/mid1),同样无法恢复靶基因的表达或抗病毒能力。重要的是,在没有病毒感染的情况下,ONAC131的敲除既没有改变MID1和D53的表达水平,也没有改变这些植株的生长发育。这些结果表明,MID1介导的抗病毒RNAi以及RDR1和RDR6的转录激活都是依赖于ONAC131的。
此外,组成型高表达ONAC131(ONAC131 CE)挽救了d14突变体植株在抗病毒RNAi中的多重缺陷。在ONAC131 CE/d14植株中,表现出较轻的疾病症状,但诱导了更高的RDR1/RDR6表达和更丰富的vsiRNA。综合上述结果表明,SL信号传导引导ONAC131的表达,ONAC131与病毒诱导的MID1协同作用,上调RDR1和RDR6的转录,从而增强vsiRNA的产生和抗病毒RNAi。
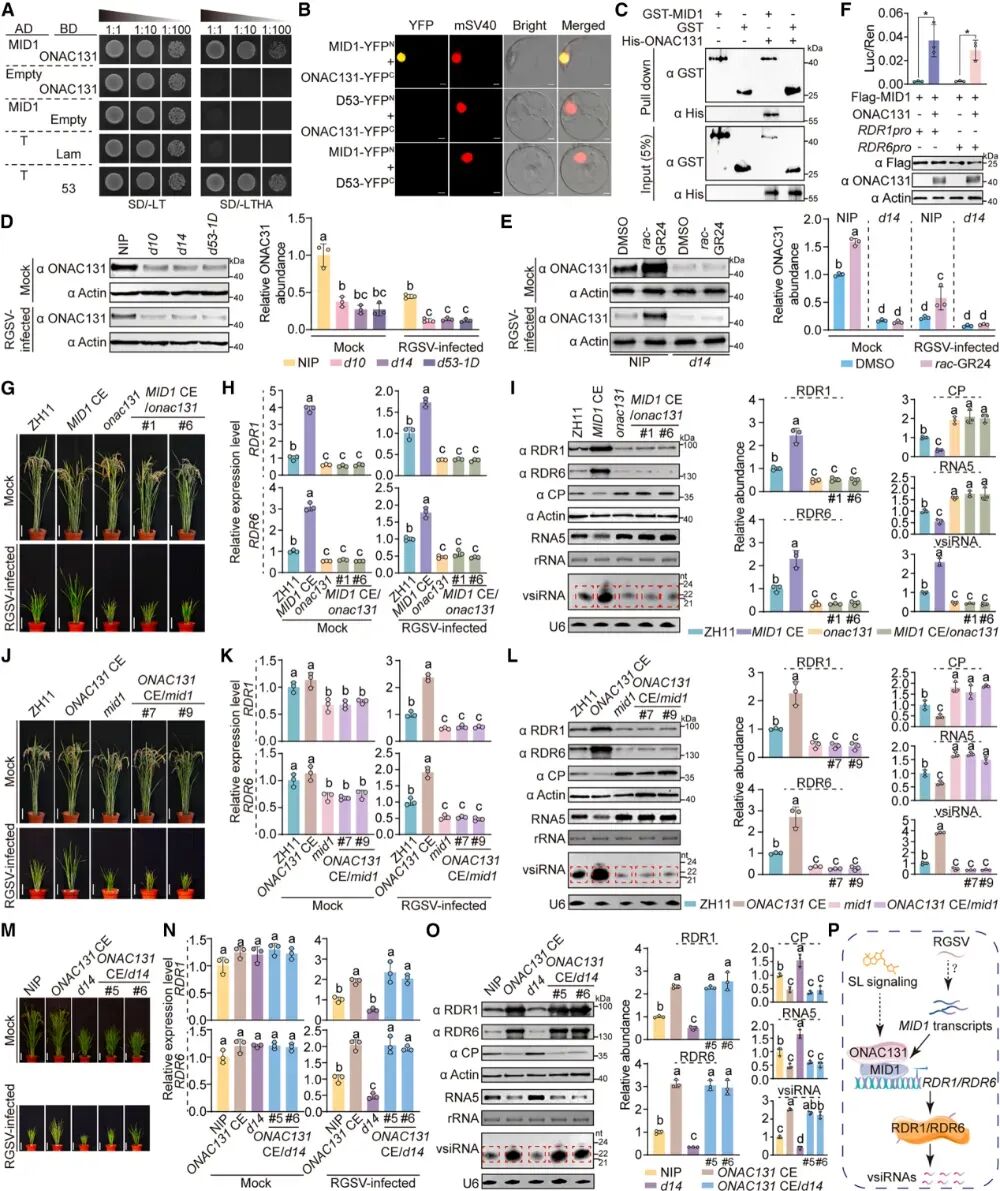
图:SL信号通路通过增强MID1相互作用蛋白ONAC131的表达来促进RDR1和RDR6的激活
四. 冷冻电镜揭示病毒通过P3蛋白占据D14的D3结合界面来抑制SL信号传导
在水稻植株中稳定表达RGSV的非结构蛋白P3,会导致水稻出现极其类似“SL信号缺陷突变体”的矮化和分蘖增多症状。研究者推测病毒P3蛋白可能直接阻断了植物的SL信号通路。为了验证这一假设,研究通过BiFC、Y2H、coIP和GST Pull-down等蛋白质互作技术,证实了病毒P3蛋白能够特异性地与植物SL激素受体D14发生物理结合。
为了看清结合细节,研究团队试图解析P3-D14复合体的晶体结构。利用冷冻电镜单颗粒分析技术(Cryo-EM SPA),研究成功解析了分辨率高达3.67Å的P3-D14异源四聚体结构。结构叠加分析揭示了一个极其巧妙的“空间位阻”机制:P3蛋白恰好占据了D14受体上原本属于核心泛素化组件D3的结合界面。这些结果表明,P3可能阻止D14招募D3,而这对于启动下游SL信号传导(例如D53降解)从而解除对SL靶基因转录激活的抑制是必需的。GST pull-down和IP结果表明,P3的介入确实阻断了D14对D3的招募;RGSV感染和病毒P3蛋白的稳定转基因表达均提高了D53的积累水平,而一旦敲除D53,就能逆转P3造成的病害表型。此外,如果在植物中引入靶向沉默P3的人工微小RNA(amivRNA3),水稻便能重新产生大量抗病毒vsiRNAs,抑制了RGSV的积累和疾病的诱发。
综上所述,这些结果表明RGSV P3通过占据D14的D3结合界面来抑制SL信号传导,从而阻断D53的降解并减弱依赖于SL的抗病毒反应。
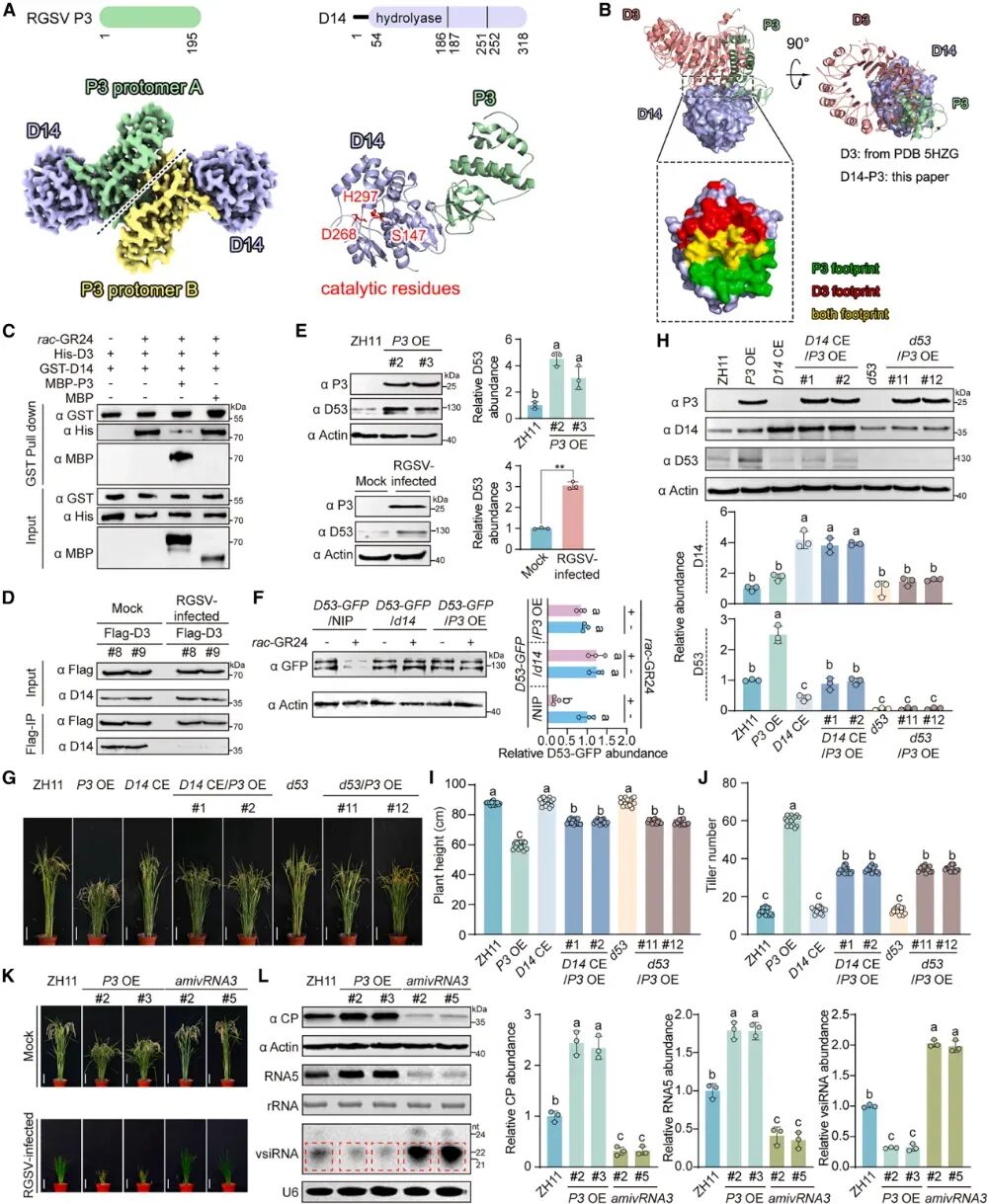
图:RGSV P3通过靶向SL受体D14抑制SL信号传导
五. D14蛋白第102位的天冬氨酸对P3相互作用至关重要,但对SL感知无影响
基于解析出的P3-D14异源四聚体结构,研究精准描绘了两者之间埋藏表面积为886.9 Ų,并详细拆解了维持该复合体的疏水作用、盐桥(如R87-E125)和氢键网络。基于P3-D14界面,研究通过定点突变生成了一系列D14突变体,包括单点替换和五个相邻残基的成簇丙氨酸(A)替换,以评估它们对P3结合的贡献。
在众多突变体中,第102位天冬氨酸突变为丙氨酸(D14D102A)展现出了令人惊叹的特性。MST和SPR显示D102A突变显著削弱了D14与病毒P3蛋白的结合力。更绝妙的是,竞争性Pull-down实验证实:与野生型D14不同,无论P3存在与否,rac-GR24触发的D14D102A对D3的招募均会发生。这意味着,这个突变消除了P3对SL信号的抑制作用。同时,另外三个界面突变体(V65A、L89A和L100A)被选中用于遗传互补测试。这些变体以及D14D102A的转基因表达,完全挽救了d14突变体的发育缺陷,其效果与野生型D14相当。
随后,研究在由D14启动子驱动表达野生型D14或抗P3的D14D102A的d14突变体植株中,分析了RGSV的感染情况。值得注意的是,与表达野生型D14的d14植株相比,在表达D14D102A的d14植株中,RGSV的积累水平更低,引起的疾病症状更轻,但诱导了更高水平的ONAC131、RDR1和RDR6表达,以及更丰富的vsiRNA。相比之下,其他仍与P3相互作用的互作界面突变体未能恢复抗性,并表现出与野生型D14相当的易感性。总之,这些发现表明,与野生型D14不同,D14D102A对P3的结合与隔离不敏感,并能保持激素感知能力以维持正常的SL信号传导,从而上调针对RGSV感染的抗病毒RNAi作用。
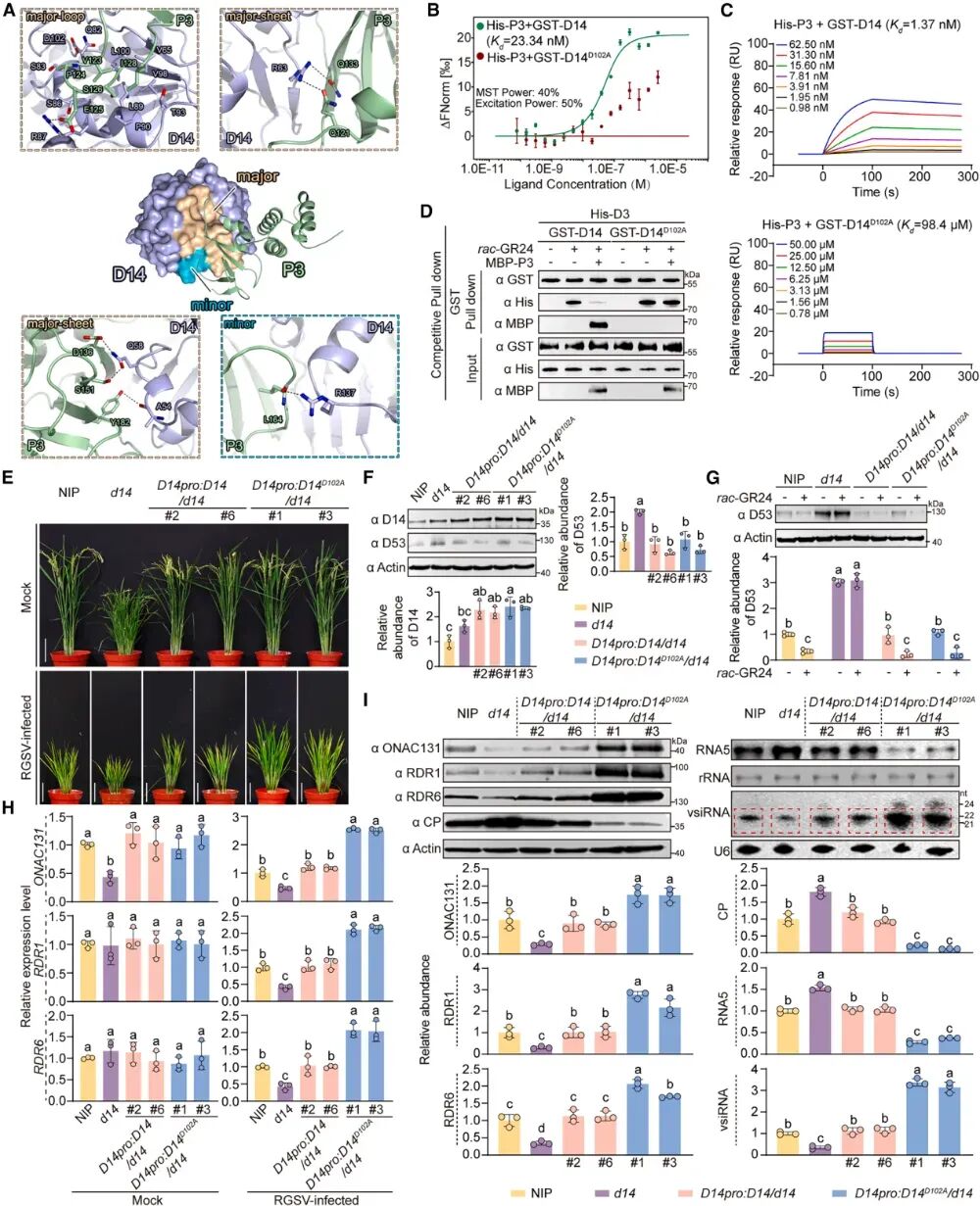
图:抗P3的D14D102A突变体表现出增强的抗病毒RNAi
六. 单核苷酸基因组编辑技术使优质水稻品种获得抗病毒性且不降低产量
研究并没有引入任何外源抗性基因,而是直接利用CBE系统,在粳稻优良品种中花11(ZH11)中,将内源D14基因的第304位胞嘧啶替换为胸腺嘧啶,从而实现了D102N的单氨基酸替换(D14D102N)。后续的Y2H和GST Pull-down生化实验再次确认这一微小的内源突变,与D14D102A一样表现出与P3的相互作用显著减弱,rac-GR24触发了D14D102N对D3的高效募集。
通过对转基因株系进行分离和筛选,在ZH11背景下获得了两个纯合编辑了D14D102N等位基因的非转基因T3代植株株系(ZH11D14(D102N))。在无病毒侵染的正常环境下:突变体与野生型的株高、分蘖数、单株产量、千粒重等核心农艺性状毫无二致。这说明内源激素的生理功能未受任何负面干扰。在RGSV病毒肆虐的水稻田中,突变体的优势比较明显。其体内的ONAC131及RDR1/6被强势激活,抗病毒vsiRNAs大量富集,病毒丰度骤降。更重要的是,在病害压力下,突变体的结实率和千粒重显著优于野生型。
为了验证该策略的普适性,研究团队将同样的D102N突变引入了中国广泛种植的籼稻主栽品种“黄华占(HHZ)”中。令人振奋的是,该策略在籼稻背景下呈现出类似表型,HHZD14(D102N) 植株发育正常且SL信号活跃,并通过逃避病毒对由SL信号上调的抗病毒RNAi的抑制作用,表现出对RGSV感染增强的抗性。
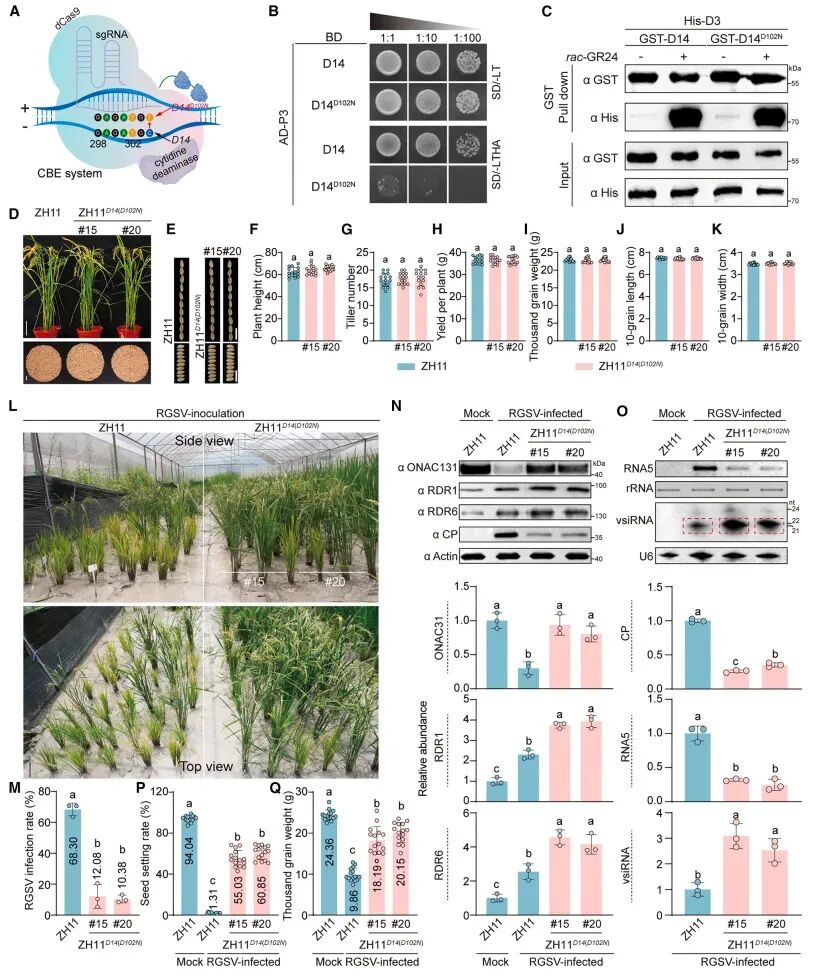
图:基于结构的D14工程增强水稻抗RGSV性而不影响产量
这项研究揭示了独脚金内酯(SL)激素信号通路在植物抗病毒RNAi防御中的核心作用,并成功提出了一种通过基因编辑培育抗病高产作物的创新策略。研究表明,SL信号通过诱导转录因子MID1与ONAC131的协同作用,激活RDR1和RDR6的表达,从而增强抗病毒小RNA(vsiRNA)的产生;然而,水稻RGSV演化出了一种反防御机制,利用其效应蛋白P3占据SL受体D14的关键结合界面,阻断正常的激素信号传导并削弱植物免疫。基于这一结构机制,研究人员利用精准的碱基编辑技术将D14受体的第102位氨基酸进行替换(D102N突变),成功阻断了病毒P3蛋白的结合,最终在不牺牲水稻产量和正常生长发育的前提下,赋予了水稻强大的广谱抗病毒能力。
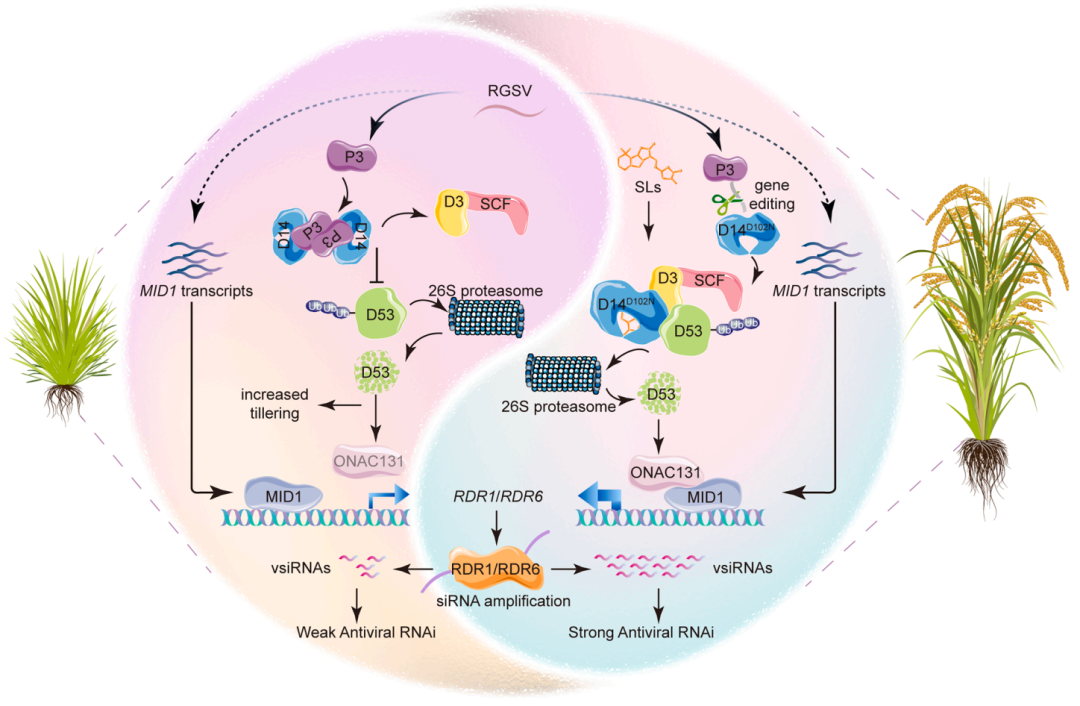
图:一种基于SL信号传导的抗病毒RNA干扰及编辑介导的病毒抑制逃逸模型
DAP-seq作为新锐之选,0抗体需求,为转录调控量身打造。爱基百客DAP-seq物种经验已有180+,相关项目文章发表在Cell、Nature Communications、Plant Cell、Developmental Cell和plant physiology等高水平期刊。欢迎咨询~
更多推荐
 已为社区贡献10条内容
已为社区贡献10条内容






所有评论(0)