“AlphaFold 4”来了?
Isomorphic Labs推出革命性AI药物设计引擎IsoDDE,Nature称其为"AlphaFold4"。该技术由诺奖得主Demis Hassabis领导开发,已与礼来、诺华等药企合作,并计划2025年开展渐冻症治疗研究。IsoDDE在蛋白质-配体结构预测、抗体抗原识别等方面表现卓越,部分指标超越现有最优模型2倍以上。不过与AlphaFold不同,IsoDDE采用闭源模
近日Google旗下的 Isomorphic Labs发布了AI药物设计新利器——Isomorphic Labs Drug Design Engine (IsoDDE),Nature号称为“AlphaFold 4”。
值得一提的是:
Isomorphic Labs的CEO为2024年诺贝尔奖化学奖获得者 Demis Hassabis。
Isomorphic Labs的核心产品包括在2024年和礼来、诺华等大药企就小分子药物发现发现展开合作,在2025年和蔡磊团队合作开发渐冻症AI治疗方案,同年宣布启动AI设计的药物进入人体临床试验阶段,其研发管线主要聚焦于肿瘤学与免疫学领域,并致力于攻克以胰腺癌、肺癌为代表的“不可成药”靶点难题。
Isomorphic Labs在2026年2月10日发布了一份长达27页的技术报告,大力宣传IsoDDE的“药物发现”能力。

报告中提到的成就——包括对蛋白质如何与潜在药物相互作用以及抗体结构的精确预测——其能力惊呆了该领域的科学家们。
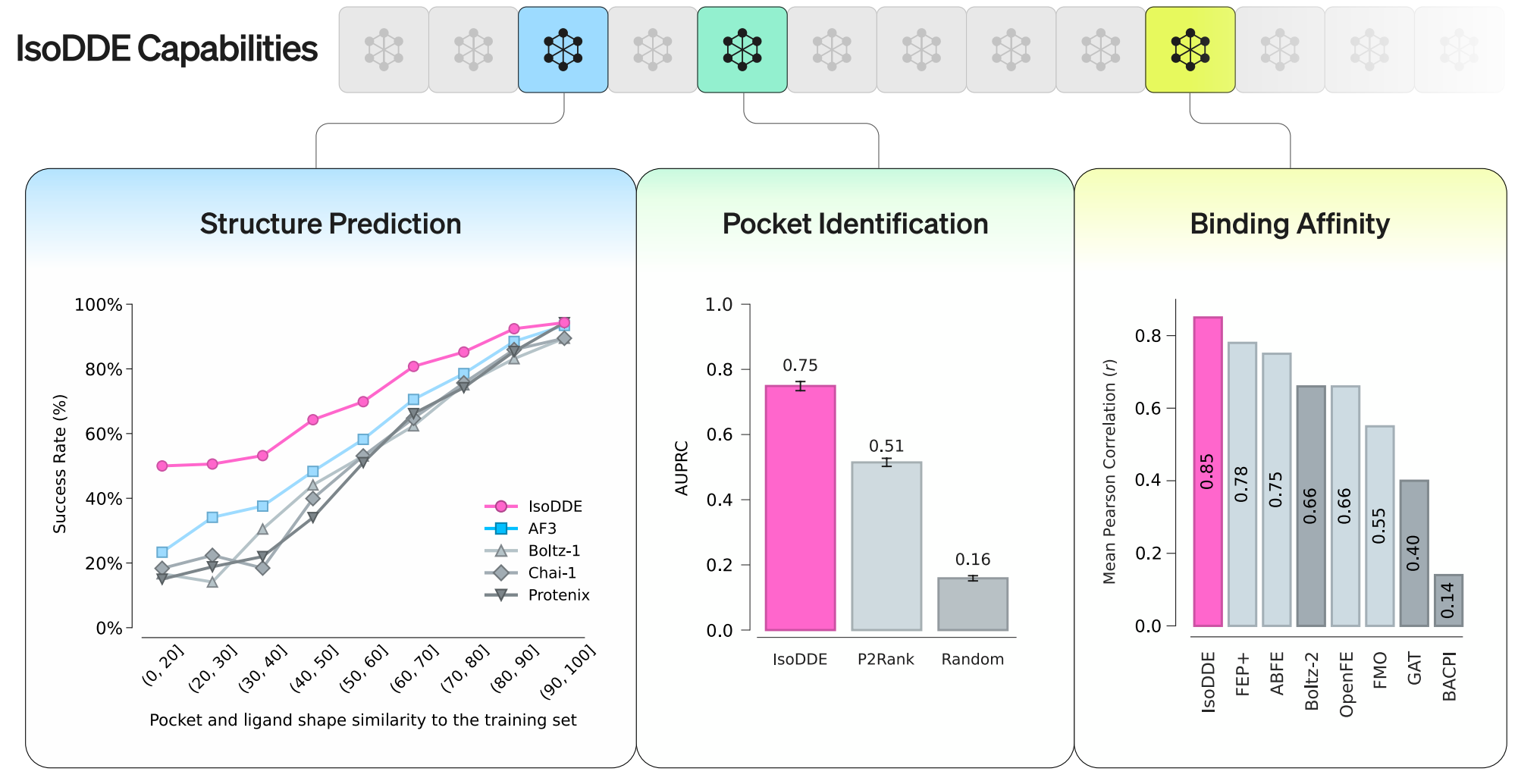
报告透露了IsoDDE在不同领域的预测能力:
- Protein-ligand structure prediction,在与训练集差异最大的Runs N’ Poses蛋白质-配体共折叠基准测试(Škrinjar et al.,2025)子集中,IsoDDE实现了比此前最优模型(AF3)超过两倍的共折叠精度提升。此外,该模型成功模拟了复杂的分布外效应——例如隐藏口袋的开启——这些效应均不在模型的训练集范围内。
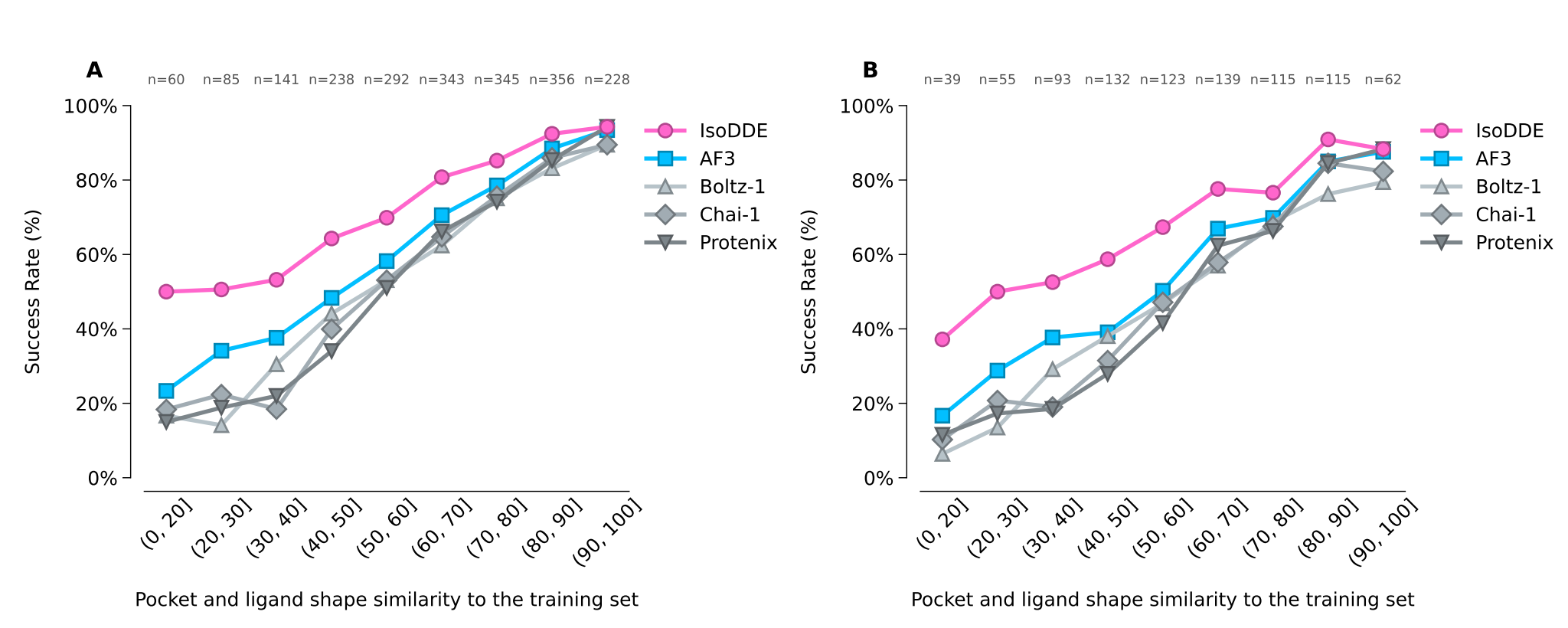
- Antibody-antigen structure prediction,在预测抗体-抗原界面时,IsoDDE展现出显著的精度提升。在一个具有挑战性的保留抗体测试集上,其高质量预测的比例超过AF3模型2.3倍,超过Boltz-2模型(Passaro et al.,2025)19.8倍。同时,IsoDDE在互补决定区重链3(CDR-H3)环的预测方面也表现出业界领先的性能(Hitawala and Gray 2025、Regep et al.2017),分别比AF3模型和Boltz-2模型提高了1.2倍和1.6倍。
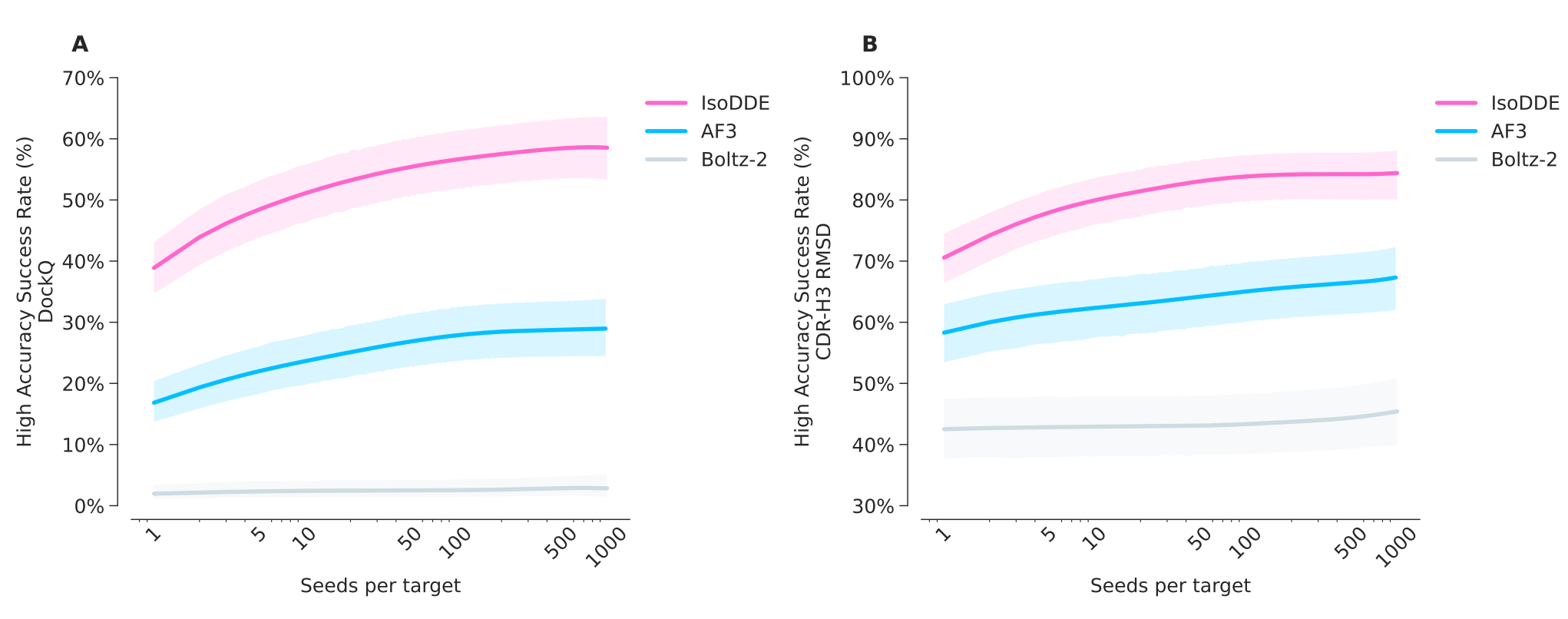
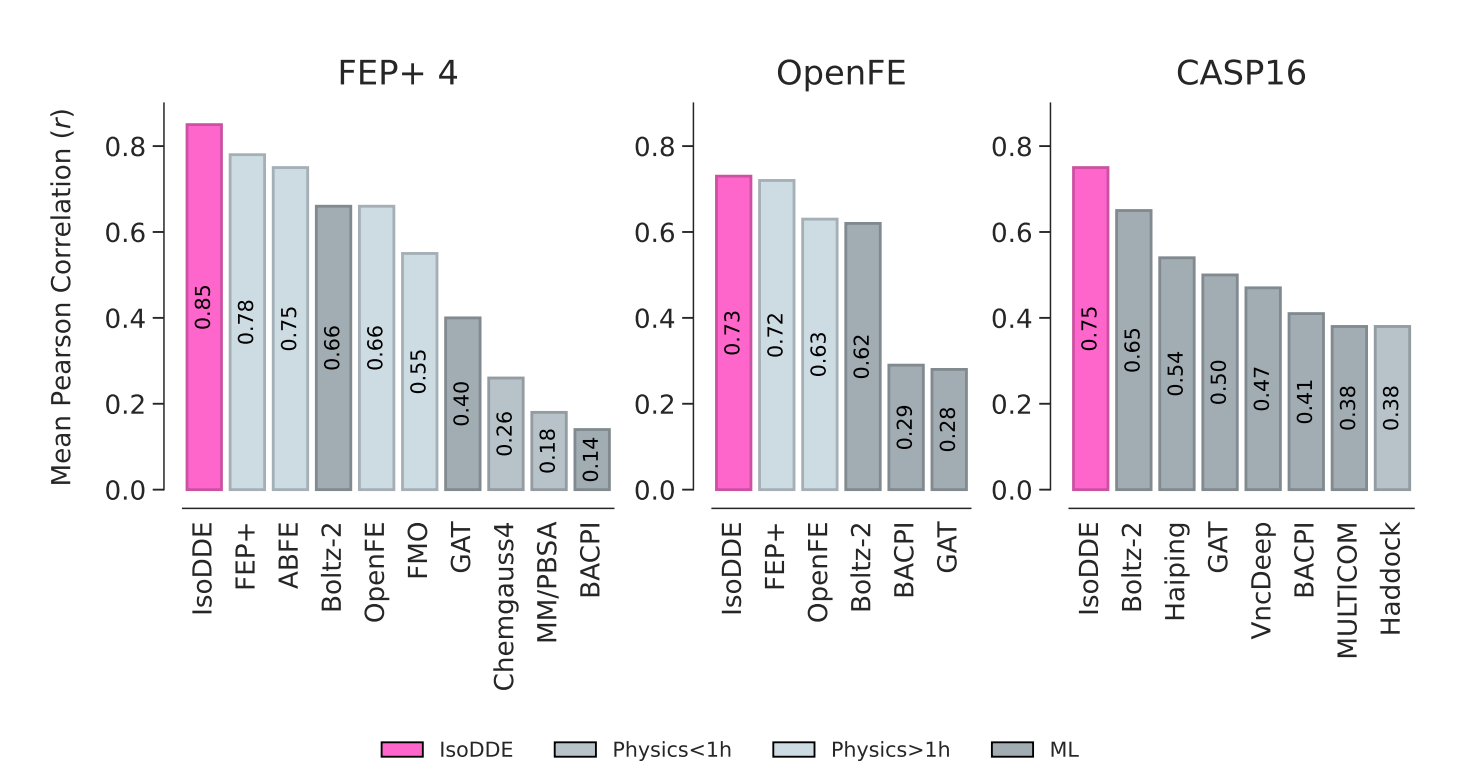
- Binding affinity,在现实药物化学基准测试中超越了当前最先进的深度学习模型,并且在适用于物理模拟的精选数据集上,其表现超越了金标准的自由能微扰方法(Passaro et al.,2025)。
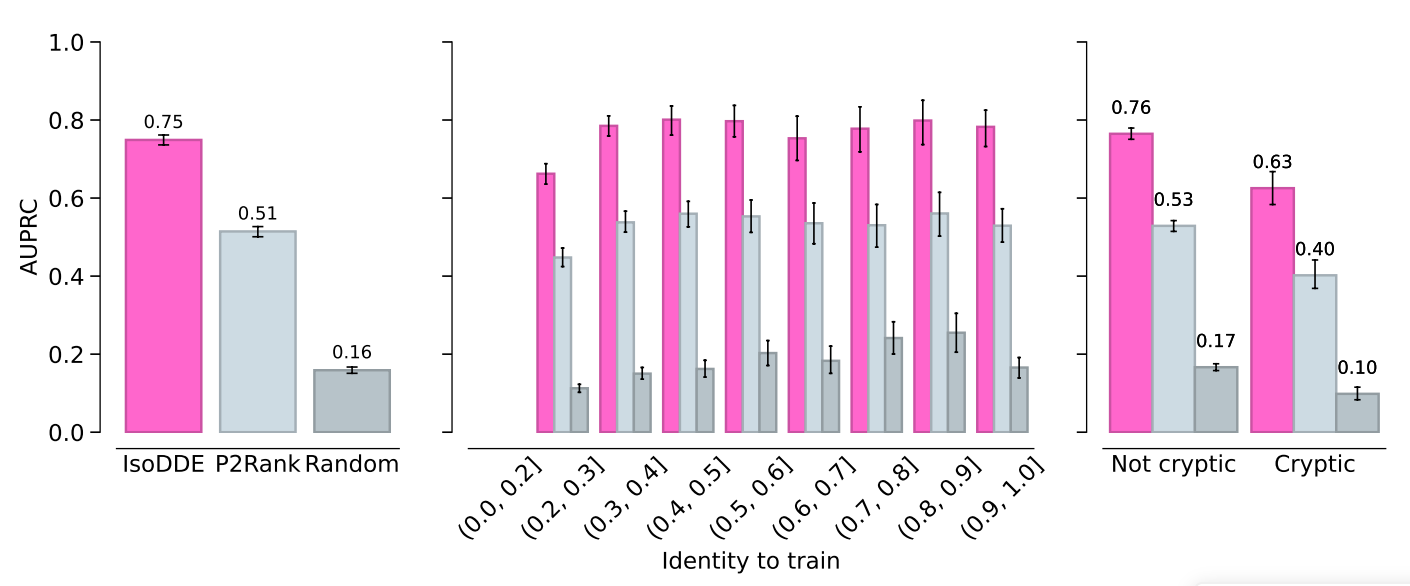
- Pocket identification,在通用测试集上,IsoDDE以1.5倍AUPRC的显著优势超越了常居榜首的开源方法P2Rank,成功识别出此前仅能通过实验方法发现的全新口袋(参考Krivák and Hoksza,2018)。
but,区别于2021年的AlphaFold2,2024年的AlphaFold3,IsoDDE不开源,技术细节也没公开。
Yet unlike the AlphaFold AI systems for predicting protein structure — which were made accessible to other researchers and described in depth in journal articles — IsoDDE is proprietary, and the technical paper offers scant insight into how to achieve similar results.
感兴趣的可以进一步学习:
-more-
《保姆级R可视化教程》来了!
嫌Matplotlib繁琐?试试Seaborn!
更多推荐
 已为社区贡献2条内容
已为社区贡献2条内容







所有评论(0)