【权威综述】骨关节炎成像2020最新进展:从传统影像到AI赋能,全面解析临床与科研应用
OA的核心病理特征是关节结构的进行性破坏,包括软骨退变、骨赘形成、半月板损伤/突出、软骨下骨硬化与囊肿、滑膜炎等。与类风湿关节炎等炎症性关节炎不同,OA的炎症多为继发性(由软骨和骨降解产物引发),其发病与生物力学异常、遗传易感性、代谢紊乱等多种因素相关。目前OA治疗仍以姑息性干预为主(缓解疼痛、改善功能),尚无根治手段。成像技术的核心价值在于:① 明确结构损伤程度,辅助临床诊断;② 捕捉早期可逆性
【权威综述】骨关节炎成像2020最新进展:从传统影像到AI赋能,全面解析临床与科研应用
骨关节炎(OA)作为全球高发的慢性退行性疾病,已成为成年人疼痛与残疾的首要原因之一。据统计,2012年全球膝OA患者已达2.5亿,随着人口老龄化与肥胖率上升,45岁以上人群中医生确诊的膝OA患病率预计将从13.8%升至15.7%。OA并非单纯的“磨损性疾病”,而是涉及软骨、半月板、滑膜、软骨下骨等多组织的全关节病变,其诊断与病情监测高度依赖成像技术。
过去十年,OA成像技术迎来爆发式发展,从传统放射学到先进的MRI、AI辅助诊断,不仅重塑了我们对OA病理机制的认知,更为临床分层、疗效评估提供了关键工具。本文基于《Radiology》2020年权威综述《State of the Art: Imaging of Osteoarthritis-Revisited 2020》,系统梳理OA成像的核心技术、临床应用与未来趋势,为放射科医师、风湿免疫科医师及相关研究者提供全面参考。
一、OA概述与成像的核心价值
1. OA的病理本质与临床挑战
OA的核心病理特征是关节结构的进行性破坏,包括软骨退变、骨赘形成、半月板损伤/突出、软骨下骨硬化与囊肿、滑膜炎等。与类风湿关节炎等炎症性关节炎不同,OA的炎症多为继发性(由软骨和骨降解产物引发),其发病与生物力学异常、遗传易感性、代谢紊乱等多种因素相关。
目前OA治疗仍以姑息性干预为主(缓解疼痛、改善功能),尚无根治手段。成像技术的核心价值在于:① 明确结构损伤程度,辅助临床诊断;② 捕捉早期可逆性病变(如软骨成分改变),为干预提供窗口;③ 量化病情进展,支撑临床试验(尤其是疾病修饰OA药物研发);④ 实现患者分层,推动精准治疗。
2. 成像技术的演进逻辑
OA成像已从“单纯评估骨结构”转向“全关节多组织评估”,从“形态学描述”转向“形态+功能+代谢”的综合评估。传统技术(放射学、超声)仍主导临床常规诊断,而MRI(含成分成像)、CT(含4D技术)、核医学及AI则成为科研与精准医疗的核心工具。
二、传统成像技术:放射学(X线)的地位与局限
放射学(X线)是OA诊断与随访的“一线标准”,至今仍是临床实践与临床试验中患者分层的核心依据,其不可替代性源于三大优势:① 普及性高、成本低、操作简便;② 能清晰显示OA的关键骨结构特征(骨赘、软骨下硬化、囊肿、关节间隙狭窄);③ 有成熟的半定量分级体系。
1. 核心评估内容与分级标准
X线评估的核心指标包括:
-
骨赘:关节边缘或中心的骨性突起,是OA最早期的放射学标志,早于关节间隙狭窄出现;
-
关节间隙狭窄(JSN):反映软骨丢失与半月板损伤/突出,是病情进展的关键指标;
-
软骨下硬化:软骨下骨密度增高,与力学负荷异常相关;
-
骨端畸形:晚期OA的特征性表现。
临床常用的分级系统有两种(表1): -
Kellgren-Lawrence(KL)分级(1958年):经典的综合分级,0-4级递进,以“明确骨赘”(KL 2级)作为放射学OA的诊断标准;
-
OARSI图谱分级:基于图像对照的分区评分,对骨赘、关节间隙狭窄进行分区域(内侧股骨髁、内侧胫骨平台等)量化,更精准但操作相对复杂。
表1:OA放射学分级系统对比
| 分级系统 | 核心特点 | 评分逻辑 |
|---|---|---|
| KL分级 | 综合评估,操作简便 | 0级(无OA特征)-4级(重度OA:大量骨赘、显著JSN、严重硬化) |
| OARSI图谱 | 分区量化,精准度高 | 骨赘(0-3分/区域)、JSN(0-3分/区域),含胫骨磨损、硬化等附加指标 |
2. 不可忽视的局限性
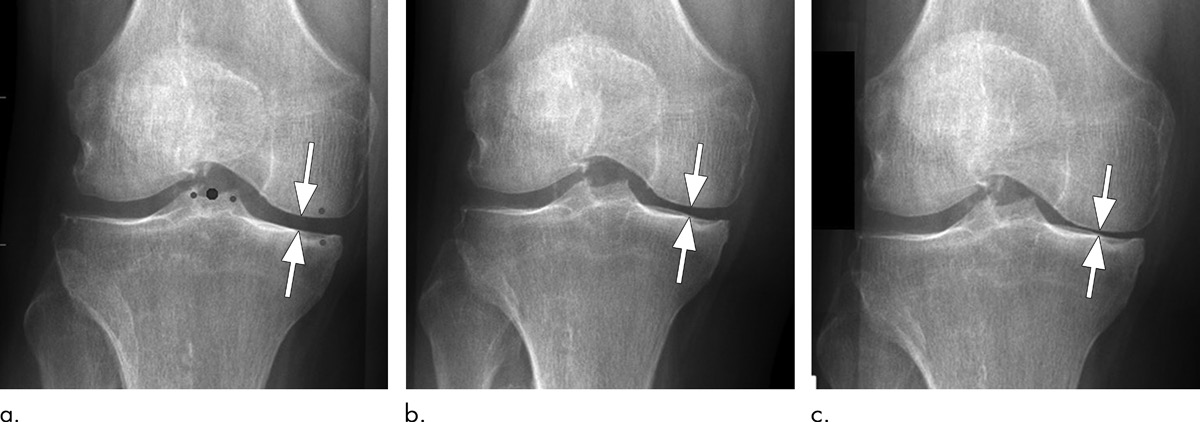
X线的短板限制了其在早期OA与软组织评估中的应用:① 对软骨、半月板、滑膜、骨髓病变等软组织不敏感,正常X线可能已存在关节内OA特征(如MRI所示的软骨损伤);② 对病情变化的敏感性低,难以监测早期进展;③ 受体位影响大(如膝关节屈曲角度差异可导致JSN假阳性/假阴性,图1);④ 仅能评估二维投影,无法反映关节三维结构与生物力学异常。
尽管如此,X线仍是FDA等监管机构推荐的III期临床试验结构终点(需通过标准化体位拍摄,如Rosenberg位45°屈曲负重位),自动化关节间隙宽度测量技术的发展已显著提升其精准度与可重复性。
三、超声成像:实时动态评估的临床优势
超声(US)凭借“实时、无辐射、低成本”的特点,成为OA临床评估的重要补充工具,尤其适用于基层医疗与床旁检查。其核心优势在于对软组织与炎症特征的高敏感性,且能实现动态成像。
1. 核心评估能力
超声可清晰显示OA的关键结构异常:
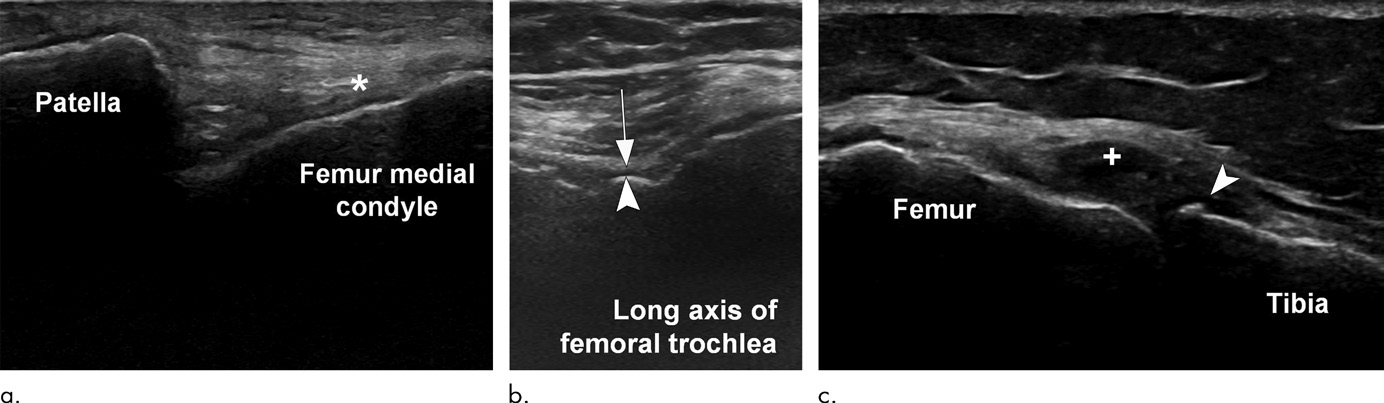
- 结构性病变:骨赘(比X线更敏感)、半月板突出(内侧半月板突出的诊断一致性高)、软骨退变(前内侧股骨髁软骨变薄/磨损的检出敏感性高,图2);
- 炎症特征:关节积液、滑膜炎(滑膜增厚、血流信号增强),且超声所示滑膜炎与OA临床症状(疼痛)、放射学进展密切相关;
- 动态评估:实时观察关节活动时的组织运动(如半月板移位、软骨接触),为生物力学异常提供线索。
2. 技术优势与局限
- 优势:无辐射、可重复检查、实时多平面成像、彩色多普勒可评估滑膜血管化,适合长期随访与大规模筛查;
- 局限:声学窗有限,难以评估关节深部结构(如胫骨内侧平台后部软骨);软骨评估仅局限于浅表区域,阴性结果不能排除退变;操作者依赖性强,诊断一致性受经验影响。
3. 临床应用场景
超声可与X线联合使用,实现OA患者的结构表型分层(如“炎症主导型”“半月板-软骨损伤主导型”),为临床试验患者筛选与治疗方案选择提供依据。在膝OA中,超声对半月板突出、滑膜炎的评估价值已得到多中心研究证实,其结果可预测关节置换风险。
四、CT与CT关节造影:骨结构与生物力学评估的新突破
CT技术的进步(尤其是 extremity锥束CT、4D CT)使其在OA评估中的价值从“单纯骨结构显示”扩展到“生物力学与软骨评估”,成为X线与MRI的重要补充。
1. 常规CT的核心应用
常规CT的优势在于骨结构的高分辨率显示:
- 精准评估骨赘大小、软骨下骨硬化范围、囊肿形态,以及钙化灶(如焦磷酸钙结晶沉积);
- 双能CT可区分半月板内的焦磷酸钙结晶与羟基磷灰石结晶,为OA病因诊断提供依据(如结晶相关OA)。
2. 先进CT技术的创新应用
- 负重位与锥束CT: extremity专用锥束CT可在负重/非负重体位下获取关节三维图像,量化关节间隙形态、半月板突出程度,且辐射剂量低于传统多排CT;
- 4D(运动)CT:时间分辨率达0.5秒,可捕捉关节运动全过程(如膝关节屈伸),评估动态生物力学异常(如髌股关节不稳定、 pisotriquetral关节不稳定),为继发性OA的病因诊断提供线索;
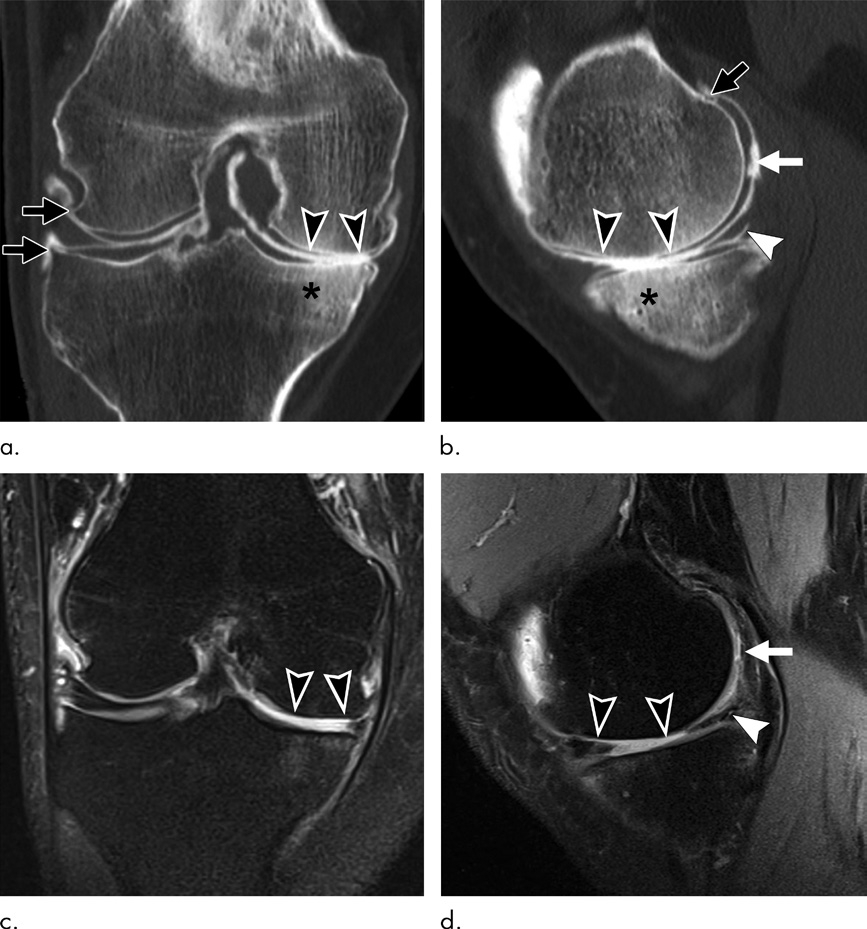
- CT关节造影(CTA):经关节内注射造影剂后,可精准评估软骨厚度、 focal软骨缺损、半月板撕裂、韧带损伤(如前交叉韧带撕裂),是软骨厚度测量的“金标准”之一(图3),且能通过无创方式评估软骨糖胺聚糖含量。
3. 局限与适用场景
- 局限:有电离辐射(不适合孕妇与儿童)、CTA为有创操作(需关节穿刺)、对软组织(滑膜、骨髓病变)的评估能力弱于MRI;
- 适用场景:OA生物力学评估(负重位/4D CT)、钙化相关OA诊断(双能CT)、软骨修复术后随访(CTA评估修复组织厚度)。
五、核医学成像:代谢层面的早期诊断价值
核医学技术(SPECT/CT、PET/CT、PET/MRI)通过评估关节代谢活动,为OA早期诊断与病理机制研究提供独特视角,尤其适用于传统影像阴性但临床症状明显的患者。
1. 核心技术与评估内容
- PET/CT/PET/MRI:18F-FDG PET可显示滑膜炎症(代谢增高),18F-NaF PET可评估软骨下骨代谢活跃程度,且软骨下骨高代谢与OA进展(软骨丢失、关节间隙狭窄)密切相关;PET/MRI融合图像可同时获得代谢信息(PET)与解剖细节(MRI),精准定位“代谢活跃+结构损伤”的区域;
- SPECT/CT:通过放射性核素聚集评估骨代谢异常,CT成分可明确病变位置(如骨赘、软骨下骨病变),但Meta分析显示其在膝OA诊断与治疗决策中的证据不足,临床应用有限。
2. 技术优势与局限
- 优势:捕捉早期代谢异常(早于结构损伤),为OA早期干预提供窗口;可评估全关节代谢状态,反映病变活动性;
- 局限:空间分辨率低、成本高、有辐射(PET/SPECT)、放射性示踪剂的 logistics 复杂,且代谢异常缺乏特异性(炎症性关节炎、创伤后修复均可导致代谢增高)。
3. 科研与临床前景
核医学技术在OA疾病修饰药物(DMOAD)临床试验中具有潜在价值,可作为“代谢终点”监测治疗对骨/滑膜代谢的影响。在ACL重建术后患者中,18F-NaF PET/MRI可检测到软骨下骨代谢增高,预测早期OA进展。
六、MRI成像:OA研究与临床的“金标准”
MRI是OA成像中最全面的技术,能同时评估关节所有组织(软骨、半月板、滑膜、骨髓、韧带),且实现“形态+成分”的综合评估,是科研(尤其是临床试验)的核心工具。
1. 半定量MRI评估:全关节病变的系统量化
半定量评分系统是MRI评估OA的基础,通过对全关节多组织病变的分级,实现病情严重程度的标准化评估,适用于纵向研究与临床试验。目前主流的评分系统有5种(表1),核心差异在于评估维度的详细程度与应用场景。
表1:OA膝关节半定量MRI评分系统对比
| 评分系统 | 发布年份 | 核心评估特征 | 评分范围 | 应用场景 |
|---|---|---|---|---|
| WORMS | 2004 | 软骨(0-6)、骨髓病变(0-3)、骨赘(0-7)、半月板撕裂(0-4)等14项指标 | 0-140分 | 基础研究、纵向随访 |
| KOSS | 2005 | 软骨(0-3)、骨髓病变(0-3)、半月板突出(0-3)等10项指标 | 0-30分 | 临床常规评估 |
| BLOKS | 2008 | 软骨(0-3)、骨髓病变(体积/面积评分)、滑膜炎症(多部位评分) | 0-100+分 | 高精度临床试验 |
| MOAKS | 2011 | 软骨(0-3)、半月板状态(撕裂/软化/囊肿)、Hoffa滑膜炎 | 0-100+分 | 药物临床试验(FDA推荐) |
| ROAMES | 2020 | 仅记录各分区最大病变等级,含排除诊断(如半月板根撕裂) | 0-3分/分区 | 临床试验患者快速筛选 |
| 这些评分系统的核心价值在于:① 实现“全关节评估”,契合OA“多组织病变”的病理本质;② 可捕捉“等级内变化”(如软骨从1级退变进展为2级),敏感性高于传统放射学;③ 评估结果与OA症状、进展风险密切相关(如骨髓病变可预测30个月内快速软骨丢失)。 |
2. 定量MRI:软骨形态的精准测量
定量MRI通过分割软骨组织,量化其厚度、体积等参数,是OA病情进展与治疗效果评估的“客观金标准”,尤其适用于DMOAD临床试验。
(1)核心技术原理
- 采用高分辨率3D序列(如FLASH、DESS),清晰区分软骨-骨界面与软骨表面;
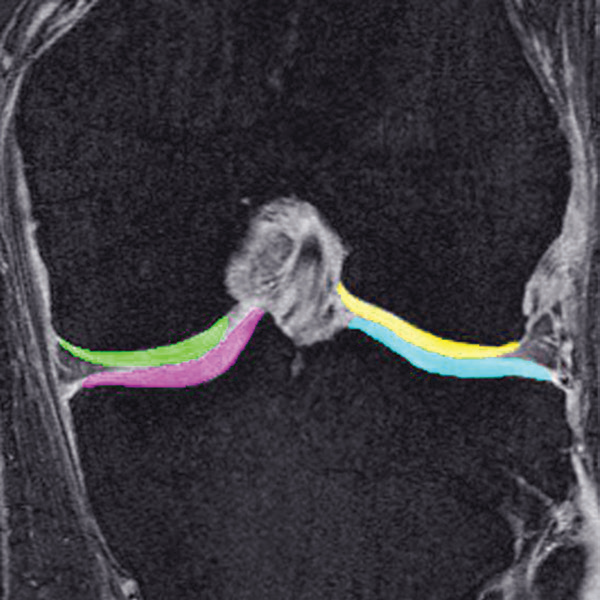
- 通过手动或自动分割(AI辅助),计算全关节软骨体积、各分区软骨厚度(图4);
- 亚区域分析可发现早期局部软骨变化(如内侧股骨髁外部软骨增厚可能是OA早期代偿表现)。
(2)临床应用价值
- 预测OA进展:基线内侧股骨软骨厚度降低是未来软骨丢失的最强预测因子;
- 治疗效果评估:已用于评估非甾体抗炎药、软骨保护剂(如硫酸软骨素)、生长因子(如sprifermin)对软骨的保护作用;
- 技术优势:客观性强、可重复性高,其敏感性显著高于放射学关节间隙狭窄测量。
3. 定量MRI:早期可逆性病变的“探测仪”
定量MRI是OA早期诊断的核心技术,可在软骨形态学改变前(X线/常规MRI阴性)检测其基质成分异常(如胶原网络破坏、蛋白多糖丢失),且这些异常具有可逆性,为干预提供关键窗口。目前已成熟的成分MRI技术包括T2 mapping、T1ρ成像、dGEMRIC等(表2)。
表2:主流定量MRI技术对比
| 技术类型 | 评估目标 | 核心优势 | 局限性 |
|---|---|---|---|
| T2 mapping | 胶原网络完整性、含水量 | 无需造影剂、易实现、基线值可预测OA进展 | 采集时间长(传统MESE序列)、受魔角效应影响 |
| T1ρ成像 | 蛋白多糖(GAG)含量 | 对早期退变敏感、可互补T2 mapping | 序列复杂(仅部分学术机构可用)、采集耗时 |
| dGEMRIC | 蛋白多糖含量 | 验证充分、可量化疾病负荷 | 需静脉注射造影剂、有肾毒性风险 |
| 钠成像 | 蛋白多糖含量 | 直接反映GAG浓度、无造影剂 | 需高场强MRI(3T+)、空间分辨率低 |
| gagCEST | 蛋白多糖含量 | 无造影剂、高特异性 | 技术复杂、验证不足、需7T MRI |
(1)关键技术解析
- T2 mapping:通过T2弛豫时间反映软骨基质状态——胶原纤维排列紊乱、含水量增加时,T2值升高。在糖尿病患者中,即使软骨形态正常,T2值也可能升高(图5),提示代谢因素对软骨的早期影响;
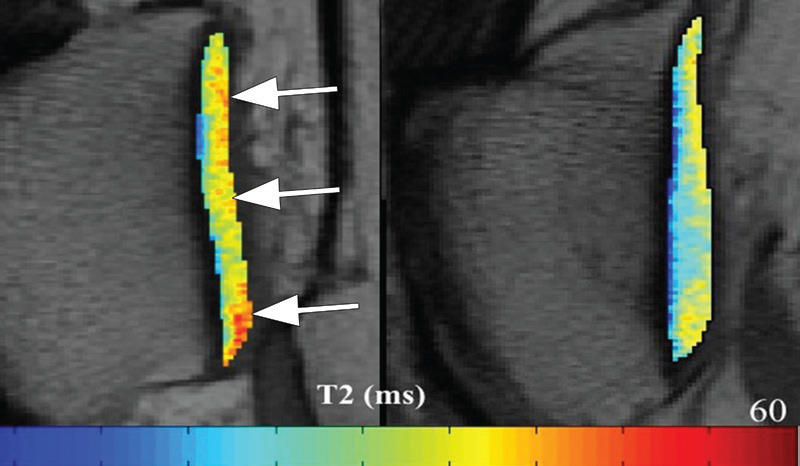
T1ρ成像:通过旋转坐标系下的T1弛豫时间评估蛋白多糖含量——蛋白多糖丢失时,T1ρ值升高,且基线T1ρ值可预测膝/髋OA进展(图6);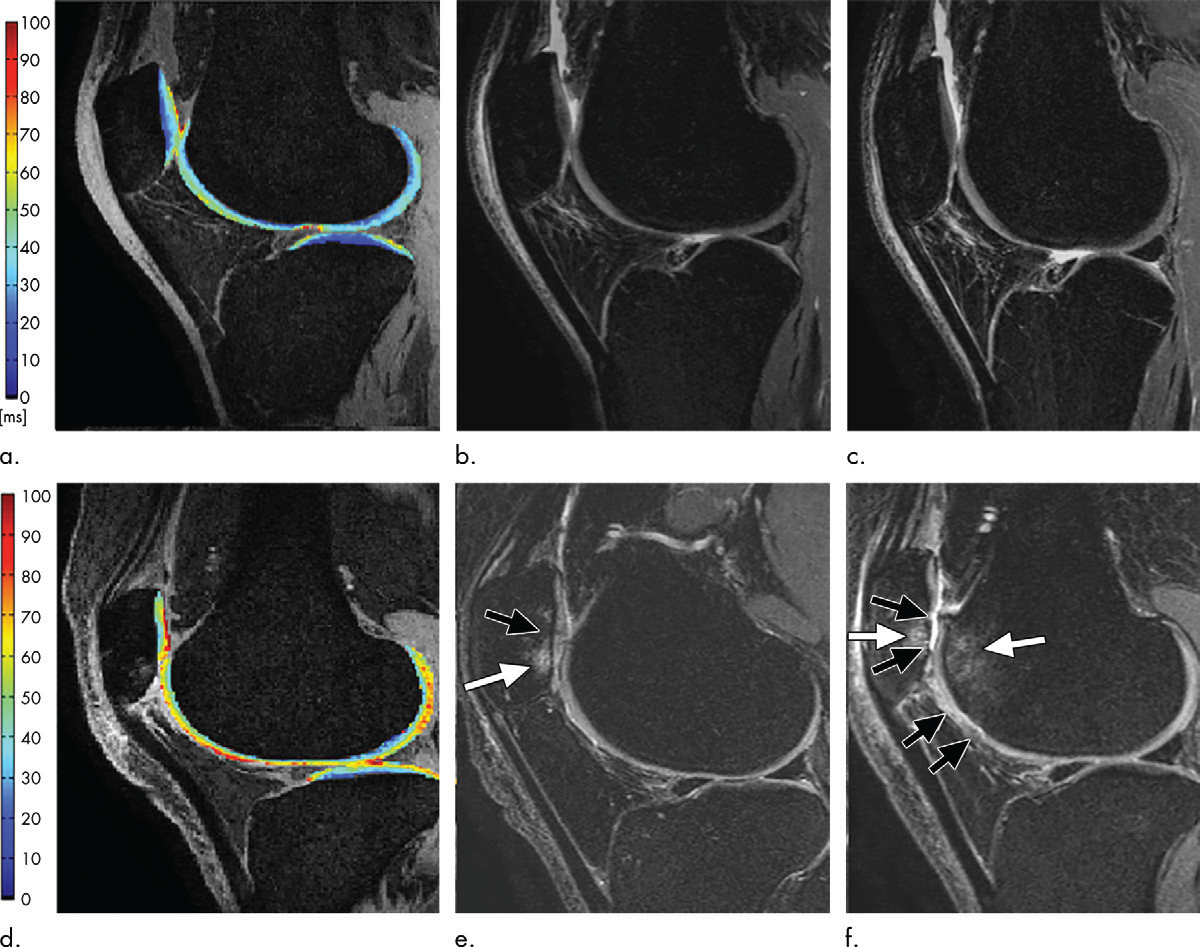
dGEMRIC:静脉注射含钆造影剂后,造影剂与软骨基质中带负电的蛋白多糖竞争结合位点,蛋白多糖丢失区域的造影剂摄取增加,T1值降低。该技术已用于发育性髋关节发育不良患者的术前评估,dGEMRIC指数异常的关节术后效果较差(图7)。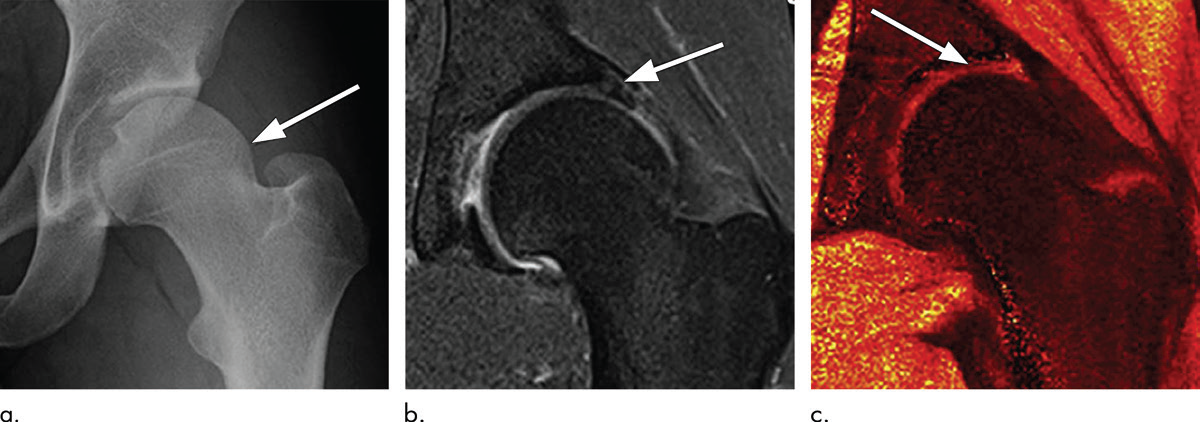
(2)临床转化前景
定量MRI的核心价值在于早期OA诊断与治疗监测。例如,T2 mapping与T1ρ成像可用于DMOAD临床试验,评估药物对软骨基质的保护作用;加速序列(如6分钟T2 mapping+形态学联合序列)的发展,已使其逐步走向临床常规应用。
七、人工智能在OA成像中的创新应用
深度学习(DL)作为人工智能的核心分支,通过多层神经网络实现图像特征的自动提取与分析,已在OA成像中展现出“高效、精准、标准化”的优势,其应用场景覆盖组织分割、疾病分级、病变检测等多个领域。
1. 核心应用方向
(1)自动化组织分割
DL可实现膝关节MRI中软骨、骨、半月板、韧带、滑膜等组织的全自动分割,相比传统 atlas-based 方法:
- 优势:速度快(分钟级完成)、计算成本低、可重复性高,适合大规模数据集分析;
- 进展:已有研究实现全关节10余种组织的同时分割,分割精度与专家手动分割相当。
(2)疾病分级与表型分类
- DL可自动对膝OA X线片进行KL分级,多中心研究显示其多分类准确率达67%,OA有无诊断的AUC达0.93;
- 基于MRI的DL模型可实现OA结构表型分类(如“炎症主导型”“骨赘主导型”),为患者分层提供依据。
(3)病变检测与预后预测
- DL可自动检测MRI中的软骨缺损、半月板撕裂、前交叉韧带损伤,诊断敏感性达69%-95%,AUC达0.80-0.91,与专家评估一致性高;
- 基于T2 maps的DL模型可区分OA与健康关节,且无需手动提取特征,诊断性能优于传统机器学习。
2. 局限与未来方向
- 目前DL模型的泛化能力依赖大规模多中心数据集,且对细微病变(如半月板根撕裂)的诊断仍需专家复核;
- 未来方向:开发“实时AI辅助诊断系统”,整合多模态影像(X线+MRI+超声)与临床数据,实现OA早期筛查、进展预测与治疗方案推荐的全流程自动化。
八、膝外关节OA成像进展(髋、手)
OA成像研究多聚焦于膝关节,但髋、手OA的患病率同样较高,其成像技术与评估逻辑具有独特性。
1. 髋OA成像
髋OA的成像挑战在于:关节位置深、软骨薄、解剖变异大(如股骨髋臼撞击症)、部分结构(如髋臼盂唇)细小。
- MRI评估:采用专用线圈与高分辨率序列,可评估软骨损伤、盂唇病变、骨髓病变、滑膜炎,主流评分系统包括HOAMS、SHOMRI(评估14项关节特征);
- 成分MRI应用:dGEMRIC已用于股骨髋臼撞击症患者的术前评估,检测早期软骨退变;
- 放射学局限:X线难以显示髋臼顶软骨损伤,正常X线可能已存在MRI所示的结构异常。
2. 手OA成像
手OA是最常见的外周OA,其成像特征与进展密切相关:
- MRI评估:滑膜炎症、骨髓病变可预测5年内关节压痛与放射学进展;
- 超声评估:滑膜增厚、关节积液、多普勒血流信号可预测2-5年的放射学进展;
- 核心价值:成像所示炎症特征(滑膜炎、骨髓病变)是手OA进展的关键预测因子,为DMOAD临床试验提供终点指标。
九、OA治疗现状与疾病修饰药物的成像关联
OA治疗的核心目标是“缓解症状、延缓进展”,成像技术不仅用于疗效评估,更在疾病修饰药物(DMOAD)研发中扮演关键角色。
1. 现有治疗方案与成像评估
- 非药物治疗:教育、运动、减重、助行器,成像可评估治疗后关节间隙狭窄速率、软骨厚度变化;
- 药物治疗:对乙酰氨基酚、NSAIDs(短期使用)、关节内注射(糖皮质激素/透明质酸),但关节内激素注射的长期安全性存疑(可能加速软骨损伤);
- 手术治疗:关节置换(晚期OA)、髋臼截骨术(发育性髋关节发育不良),术前成像(如dGEMRIC)可预测手术效果。
2. DMOAD研发与成像终点
目前尚无获批的DMOAD,但多项药物处于III期临床试验阶段,成像技术是其疗效评估的核心终点:
- 神经生长因子(NGF)抗体:如tanezumab,可显著缓解OA疼痛,MRI用于监测是否出现快速进展性OA;
- 生长因子:如sprifermin(成纤维细胞生长因子18),可增加股骨胫骨关节软骨厚度(MRI定量测量证实);
- 成像终点:FDA推荐将“关节间隙狭窄速率”“软骨体积变化”“成分MRI参数(如T2值)”作为DMOAD临床试验的核心终点。
十、展望:成像技术驱动OA精准医疗的未来
OA成像的未来发展将聚焦于“早期诊断、精准分层、治疗监测”三大目标,核心趋势包括:
- 多模态融合:整合X线(骨结构)、超声(炎症)、MRI(形态+成分)、核医学(代谢)数据,构建OA“全维度评估模型”,实现早期诊断与病理机制解析;
- AI赋能的标准化:开发临床可用的AI辅助诊断系统,自动化完成分割、分级、病变检测与预后预测,降低操作者依赖性,推动大规模筛查与多中心研究;
- 成分MRI的临床普及:加速序列(如5分钟DESS序列同时实现形态与T2定量)的发展,使成分MRI从科研走向临床常规,成为早期OA筛查工具;
- DMOAD的成像伴随诊断:基于成像表型(如“成分异常型”“炎症主导型”)筛选适合特定DMOAD的患者,实现精准治疗;
- 跨关节成像技术统一:建立髋、手、踝等关节的标准化成像协议与评分系统,推动OA全关节评估的规范化。
参考文献
Roemer FW, Demehri S, Omoumi P, et al. State of the Art: Imaging of Osteoarthritis-Revisited 2020[J]. Radiology, 2020, https://doi.org/10.1148/radiol.2020192498.
欢迎关注
微信:Chushanzhishi2022
微信公众号:NMR凯米小屋
作者B站:楚山之石
更多推荐
 已为社区贡献2条内容
已为社区贡献2条内容







所有评论(0)