肿瘤预测TIDE的使用
http://tide.dfci.harvard.edu/login/用edu邮箱进行注册。input有需要进行标准化。input教程:【预测抗PD1和抗CTLA4免疫治疗反应的在线网站工具使用方法】TIDE: TumorImmuneDysfunction andExclusion_哔哩哔哩_bilibiliTIDE算法来预测免疫治疗疗效 – 王进的个人网站 (jingege.wang)在线分析得
目录
在线网站
用edu邮箱进行注册。Tumor Immune Dysfunction and Exclusion (TIDE) (harvard.edu)
input有需要进行标准化。input教程:
【预测抗PD1和抗CTLA4免疫治疗反应的在线网站工具使用方法】TIDE: Tumor Immune Dysfunction and Exclusion_哔哩哔哩_bilibili
TIDE算法来预测免疫治疗疗效 – 王进的个人网站 (jingege.wang)
在线分析得出结果解读:
肿瘤TIDE在线分析结果中各项的具体含义如下:
-
No benefits: 表示该肿瘤样本在免疫治疗中没有受益,即患者对免疫治疗的反应不明显。
-
Responder: 表示该肿瘤样本对免疫治疗有积极的反应,可能对免疫治疗有较好的效果。
-
TIDE: Tumor Immune Dysfunction and Exclusion(肿瘤免疫功能障碍和排斥)的缩写,是一种衡量肿瘤免疫治疗反应的指标。它可以评估肿瘤细胞、免疫细胞和免疫逃逸机制之间的相互作用。
-
IFNG: interferon gamma(干扰素γ),是一种由免疫细胞产生的细胞因子,对免疫活性具有重要作用。
-
MSI Expr Sig: Microsatellite Instability Expression Signature(微卫星不稳定性表达标记),用于评估肿瘤基因组的微卫星不稳定性程度。微卫星不稳定性与免疫治疗的反应之间存在关联。
-
Merck18: Merck18 gene signature(Merck18基因签名),是一种用于预测免疫检查点抑制剂治疗反应的基因组标记。
-
CD274: Cluster of Differentiation 274,也称为PD-L1(Programmed Death-Ligand 1),是一种免疫检查点分子,与免疫治疗的效果相关。
-
CD8: Cluster of Differentiation 8,也称为CD8+ T淋巴细胞。CD8+ T细胞是一种重要的免疫细胞,与抗肿瘤免疫反应有关。
-
CTL.flag: Cytotoxic Lymphocyte(细胞毒性淋巴细胞)标志物,用于评估肿瘤浸润淋巴细胞的情况。
-
Dysfunction: 免疫功能障碍,指免疫系统在抵抗肿瘤时受到抑制或功能异常。
-
Exclusion: 免疫排斥,指肿瘤细胞阻止免疫细胞进入肿瘤微环境,从而逃避免疫攻击。
-
MDSC: Myeloid-Derived Suppressor Cells(髓系来源的抑制性细胞),是一类免疫抑制细胞,可以抑制免疫细胞的活性。
-
CAF: Cancer-Associated Fibroblast(癌相关成纤维细胞),是一种存在于肿瘤组织中的纤维细胞,参与肿瘤的生长和进展。
-
TAM M2: Tumor-Associated Macrophage M2(肿瘤相关巨噬细胞M2型),是一种类型的巨噬细胞,与肿瘤免疫逃逸和免疫抑制有关。
免疫队列
-
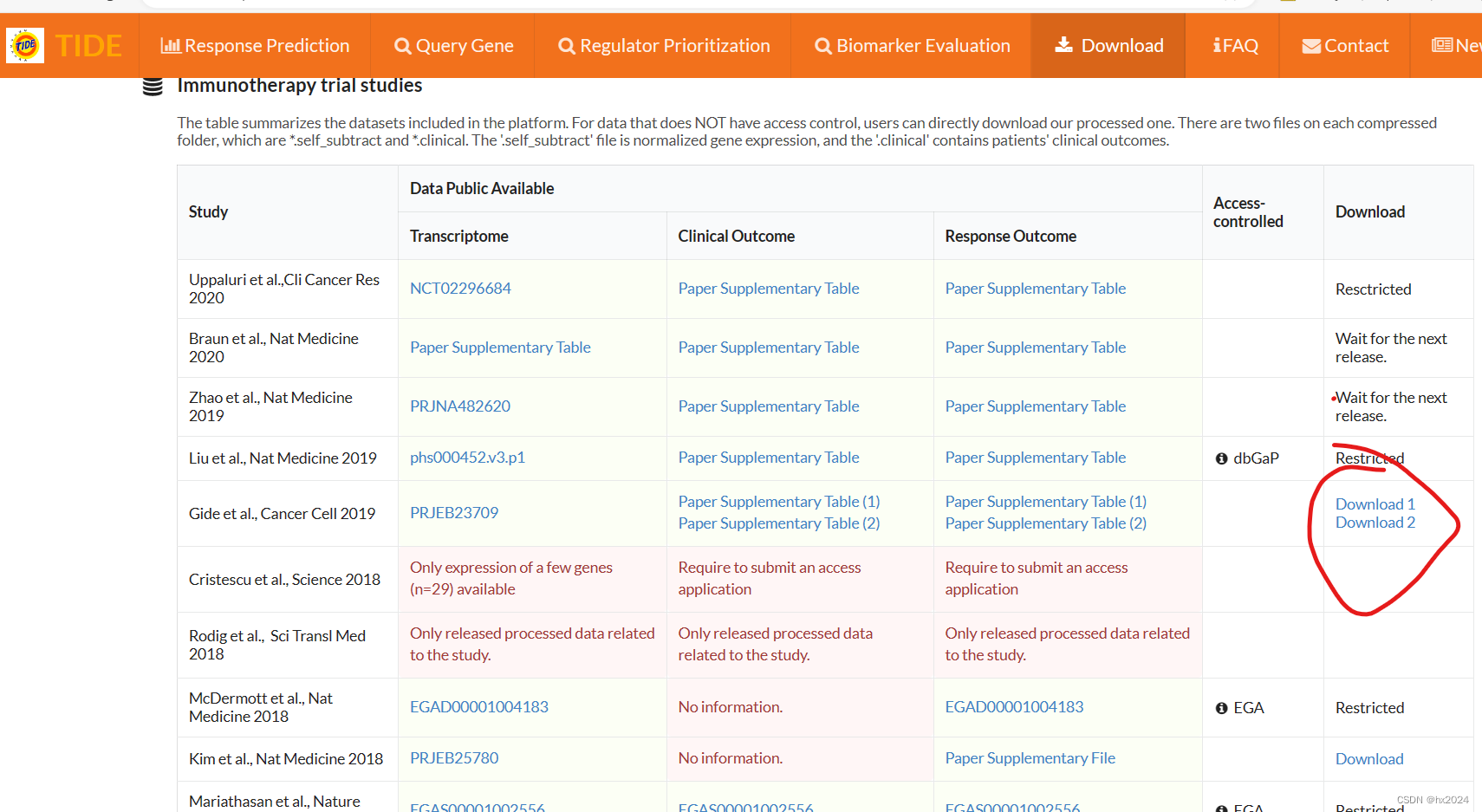
TIDE数据库还可以下载很多免疫治疗队列的表达矩阵进行分析
Tumor Immune Dysfunction and Exclusion (TIDE) (harvard.edu)
例如:GSE93157队列。Programmed death 1 receptor blockade and immune-related gene expression profiling in non-small cell lung carcinoma, head and neck squamous cell carcinoma and melanoma。GEO Accession viewer (nih.gov)
也可以从TIDE网页下载表达矩阵。
包括的免疫治疗队列
|
ICB Cohorts |
Data Public Available |
# of Patients (Not Available) |
# of Patients (Included) |
||
|
Transcriptome |
Response Outcome |
Survival Outcome |
|
|
|
|
Van Allen et al., Science 2015 [1] |
Yes |
Yes |
Yes |
|
42 |
|
Chen et al., Cancer Discov 2016 [2] |
Yes |
Yes |
No |
|
33 |
|
Hugo et al., Cell 2016 [3] |
Yes |
Yes |
Yes |
|
25 |
|
Lauss et al., Nat Commun 2017 [4] |
Yes |
Yes |
Yes |
|
28 |
|
Ayers et al., J Clin Invest 2017 [5] |
No |
No |
No |
81 |
\ |
|
Prat et al., Cancer Res 2017 [6] |
Yes |
Yes |
Yes |
|
33 |
|
Nathanson et al., Cancer Immunol Res 2017 [7] |
Yes |
Yes |
Yes |
|
24 |
|
Riaz et al., Cell 2017 [8] |
Yes |
Yes |
Yes |
|
51 |
|
Miao et al., Science 2018 [9] |
Yes |
Yes |
Yes |
|
33 |
|
Mariathasan et al., Nature 2018 [10] |
Yes |
Yes |
Yes |
|
348 |
|
Kim et al., Nat Medicine 2018 [11] |
Yes |
Yes |
No |
|
45 |
|
McDermott et al., Nat Medicine 2018 [12] |
Yes |
Yes |
No |
|
263 |
|
Rodig et al., Sci Transl Med 2018 [13] |
No |
No |
No |
181 |
\ |
|
Cristescu et al., Science 2018 [14] |
No |
No |
No |
315 |
\ |
|
Gide et al., Cancer Cell 2019 [15] |
Yes |
Yes |
Yes |
73 |
|
Table S2. Data availability of published ICB studies. All studies are annotated separately by the availability of transcriptomic data, response outcome, and survival outcome.
注意表达矩阵处理方法
下载的表达矩阵含有负值
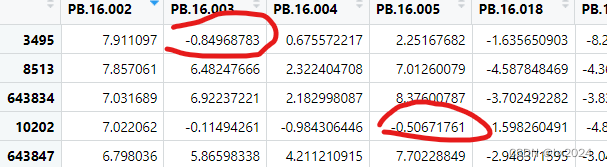
处理方式:For each RNA-seq dataset, the transcriptomic profile was log2(1+TPM) transformed. We standardized the log scale transcriptome data across patients by quantile-normalization, and further normalized the expression values of each gene by subtracting the average among all samples. 对于每个 RNA-seq 数据集,转录组概况都进行了 log2(1+TPM)转换。我们通过量化归一化对患者的对数尺度转录组数据进行标准化,并通过减去所有样本的平均值进一步归一化每个基因的表达值。(有两次转换)
所以下载的表达矩阵是经过归一化后的值。
更多推荐
 已为社区贡献6条内容
已为社区贡献6条内容







所有评论(0)